Unter einer Zelle versteht man eine kleine, dreidimensionale, lebende Struktur. Ihr Inneres ist mit einer wässrigen Lösung gefüllt, in der zahlreiche (bio-)chemische Vorgänge ablaufen, und nach außen wird sie durch eine dynamische, bewegliche Hülle abgegrenzt. Damit ist die Zelle die kleinste Einheit, in der Leben organisiert stattfinden kann.
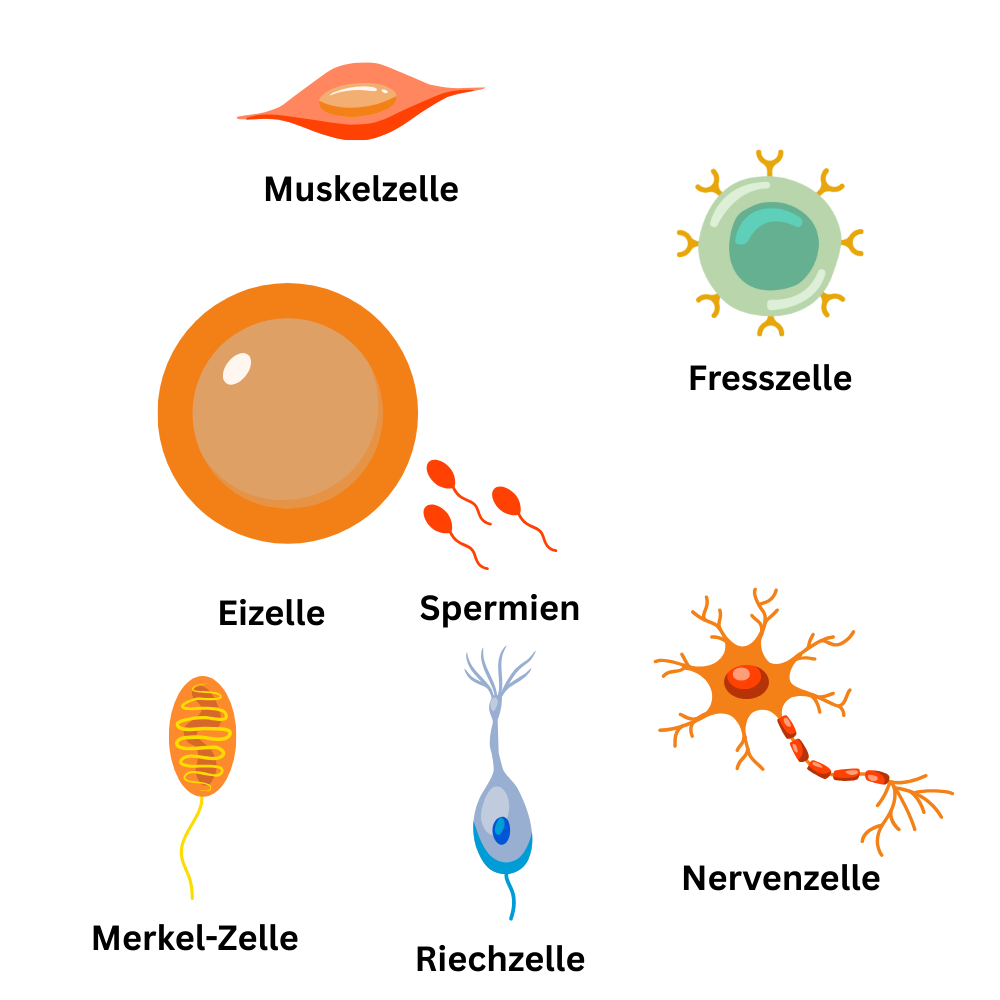
Wichtig ist dabei: Der Begriff „Einheit des Lebens“ bedeutet nicht, dass Zellen alle gleich wären. Im Gegenteil unterscheiden sie sich – vor allem in Vielzellern – teils deutlich in Form und Funktion. Körperzellen beim Menschen sind (mit wenigen Ausnahmen) stark spezialisiert, was man an ihrer großen Vielfalt gut erkennt.
Gemeinsamkeiten und Unterschiede von Zellen #
Trotz dieser Vielfalt besitzen Zellen grundlegende gemeinsame Bausteine. Dazu zählen vor allem die Zellorganellen, also funktionelle Struktureinheiten, die in (fast) allen Zellen vorkommen. Um die Zelle als Gesamtsystem zu verstehen, ist es sinnvoll, zuerst den allgemeinen Aufbau und die Grundfunktionen zu klären und anschließend die einzelnen Organellen Schritt für Schritt zu vertiefen.
Als erste Orientierung teilt man Zellen grob in zwei Gruppen ein: Prokaryoten und Eukaryoten. Prokaryoten sind im Vergleich einfacher organisiert und besitzen keinen Zellkern; ihre wichtigsten Vertreter sind die Bakterien. Eukaryoten sind durch einen Zellkern gekennzeichnet und umfassen unter anderem Tiere, Pflanzen und Pilze.
Für das Textverständnis ist außerdem hilfreich, typische Wortbestandteile zu erkennen: „pro-“ wird häufig im Sinn von „vor“ verwendet, „kary-“ bezieht sich auf den Kern, „zyto-“ auf die Zelle. Auch die Präfixe „intra-“, „inter-“ und „extra-“ sind in der Biologie ständig präsent und bedeuten „innerhalb“, „zwischen“ bzw. „außerhalb“ (z. B. intrazellulär, interzellulär, extrazellulär).
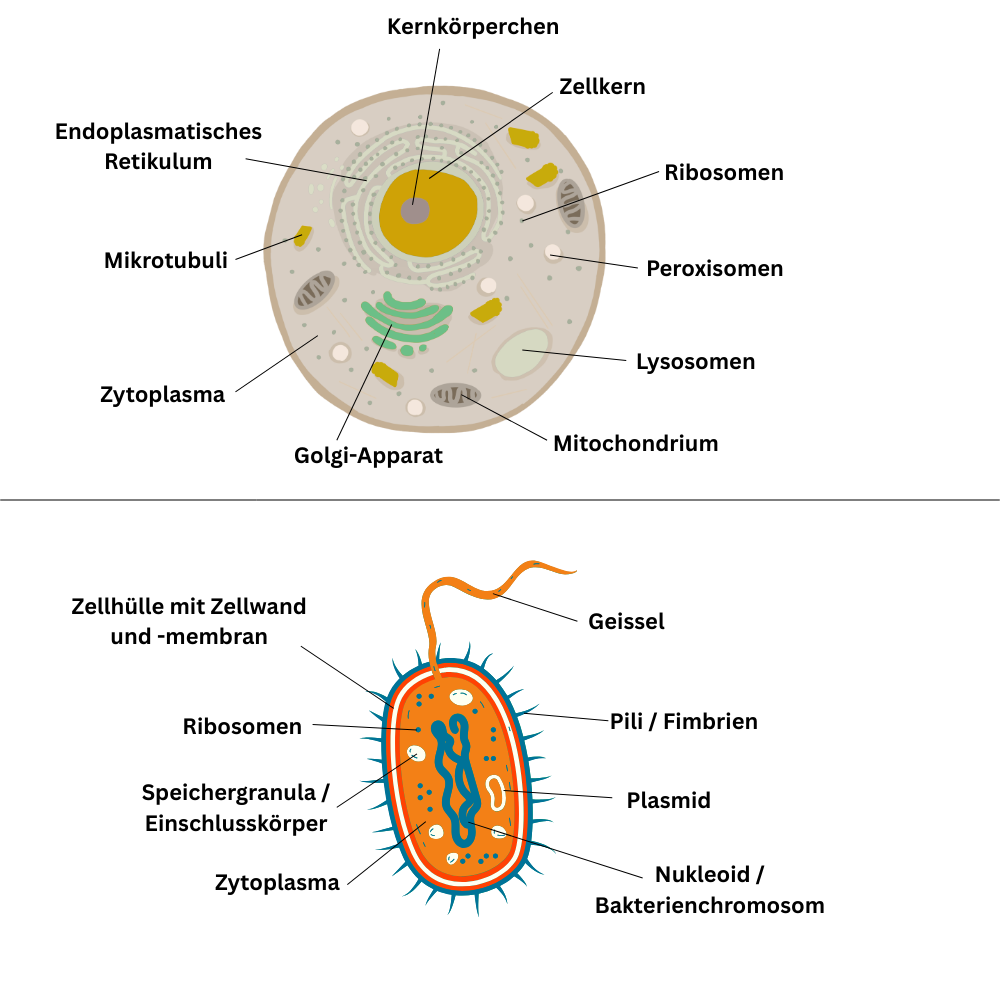
Was kennzeichnet nun die eukaryotische Zelle grundsätzlich? Sie bildet einen durch die Zellmembran abgegrenzten Raum, in dem Stoffwechsel abläuft. Dieser Raum ist nicht leer, sondern enthält das Zytosol als wässrige Grundlösung. Die Zelle ist dabei nicht einfach „flüssig gefüllt“, sondern erhält Form und Stabilität durch das Zytoskelett, ein Netzwerk aus ineinandergreifenden Proteinstrukturen, das mit Organellen und Zellmembran in Verbindung steht.
Aus diesem zellulären Gerüst können Oberflächenstrukturen hervorgehen, etwa Kinozilien, Geißeln oder Mikrovilli. Je nach Ausprägung vergrößern sie die Oberfläche oder ermöglichen bestimmte Bewegungs- bzw. Transportfunktionen an der Zelloberfläche.
Zellen stehen außerdem immer in einem Umfeld: Eukaryotische Zellen werden von Interzellularflüssigkeit umspült, die unter anderem der Ernährung und Kommunikation dient. Zwischen den Zellen liegt der Interzellularraum, der nicht leer ist, sondern auch durch Interzellularsubstanz/extrazelluläre Matrix geprägt sein kann, welche Geweben mechanische Struktur verleiht.
Ein zentrales Organell der Eukaryoten ist der Zellkern als Hauptspeicher der DNA. Zusätzlich findet sich DNA in den Mitochondrien, die die notwendige Energie für den Stoffwechsel bereitstellen. Für Herstellung, Modifikation und Sortierung von Zellprodukten sind insbesondere endoplasmatisches Retikulum und Golgi-Apparat wichtig; für Abbauprozesse stehen Systeme wie Lysosomen, Proteasomen und Peroxisomen zur Verfügung.

Die Funktionen einer Zelle ergeben sich damit aus dem Zusammenspiel ihrer Bestandteile. Zu den grundlegenden Eigenschaften, die Zellen als „lebendig“ kennzeichnen, zählen vor allem Vermehrung (im Rahmen des Zellzyklus), Stoffwechsel, Reizaufnahme und -verarbeitung, Beweglichkeit, außerdem Strukturiertheit, Wachstum/Entwicklung sowie der Zelltod (z. B. Apoptose oder Nekrose).
Der Begriff Stoffwechsel (Metabolismus) fasst die Gesamtheit der chemischen Vorgänge in der Zelle zusammen. Ziel ist der Aufbau und Erhalt der Zellsubstanz sowie die Bereitstellung von Energie für energieverbrauchende Prozesse, etwa die Kontraktion von Muskelzellen.
Dabei gilt: Nicht jede Zellart muss jede dieser Eigenschaften gleich stark ausprägen. Welche Funktionen dominieren, hängt von der Spezialisierung und der entsprechenden Ausstattung mit Organellen ab – eine Knochenzelle hat andere Anforderungen als bewegliche Zellen des Immunsystems.
Zellmembran #
Die Zellmembran (auch Plasmamembran) ist eine extrem dünne Grenzschicht von etwa 5 nm, die die Zelle nach außen abgrenzt. Sie besteht im Wesentlichen aus Lipiden und Proteinen. Lipide sind dadurch gekennzeichnet, dass sie in Wasser nur schlecht löslich sind (hydrophob), während Proteine aus Aminosäuren aufgebaute Makromoleküle sind, deren Zusammensetzung durch die genetische Information festgelegt wird.
Ihre Funktion geht deutlich über „Hülle der Zelle“ hinaus. Membranen ermöglichen in der Zelle die Kompartimentierung, also die Bildung abgegrenzter Räume. Dadurch können bestimmte Stoffe lokal angereichert werden, was viele Reaktionen überhaupt erst effizient macht. Außerdem sind Membranen zentral, wenn es darum geht, Konzentrationsgradienten aufzubauen und zu erhalten – beispielsweise für Energieprozesse (z. B. in Mitochondrien) oder für die elektrische Signalweiterleitung in erregbaren Zellen.
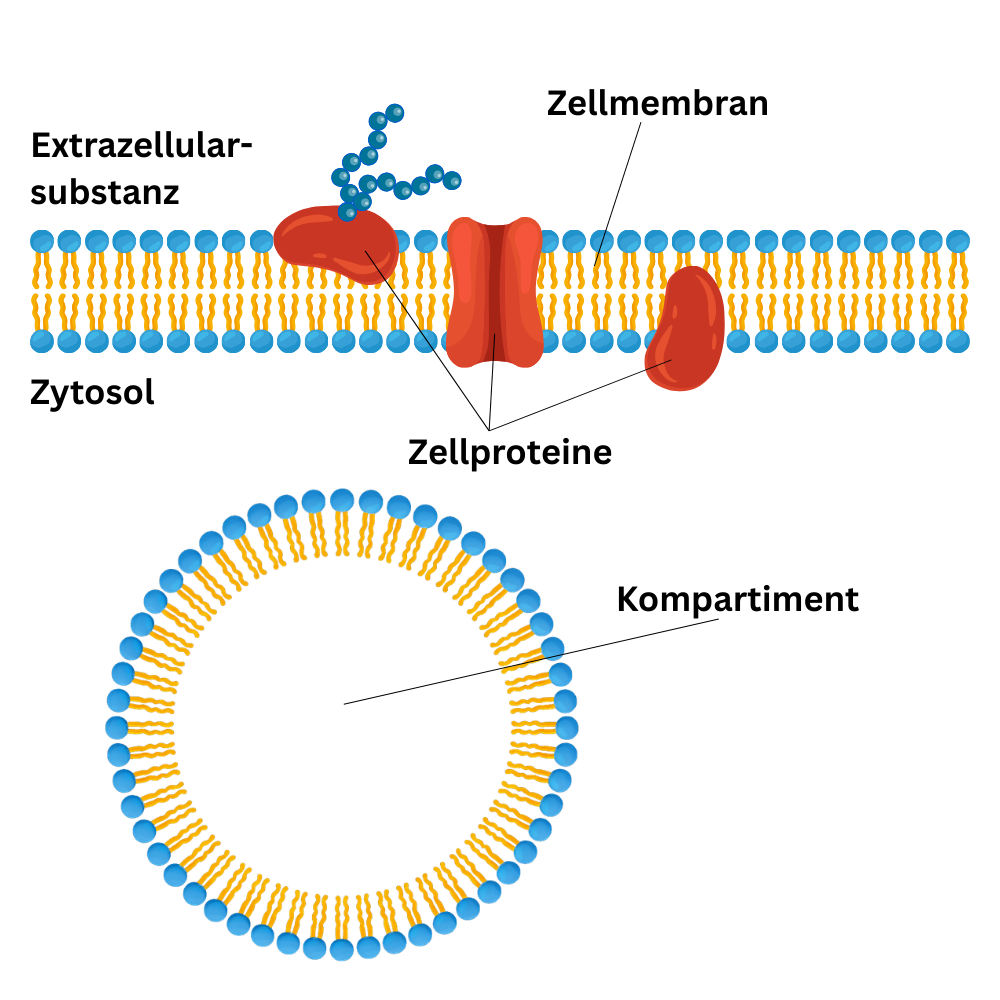
Da Membranen in der Zelle nach einem ähnlichen Grundprinzip gebaut sind, spricht man oft von biologischen Einheitsmembranen. Der wichtigste strukturelle Baustein dabei ist das Phospholipid.
Um den Aufbau zu verstehen, ist die Unterscheidung folgender Begriffe hilfreich: lipophil/hydrophob/apolar beschreibt Stoffe, die „fettliebend“ sind und Wasser eher meiden. lipophob/hydrophil/polar beschreibt Stoffe, die gut mit Wasser wechselwirken. Amphiphile Moleküle besitzen beides: einen wasserliebenden und einen fettliebenden Anteil – genau das trifft auf Phospholipide zu. Sie tragen einen polaren, hydrophilen Kopf (Phosphatgruppe) und zwei unpolare, hydrophobe Schwänze (Kohlenwasserstoffketten, meist Fettsäuren).
Struktur der Zellmembran
Weil sowohl außerhalb der Zelle als auch im Zellinneren Wasser das dominierende Lösungsmittel ist, richtet sich die Anordnung der Phospholipide immer so aus, dass der Kontakt „passt“: Hydrophile Köpfe orientieren sich zum Wasser, hydrophobe Schwänze vermeiden Wasser.
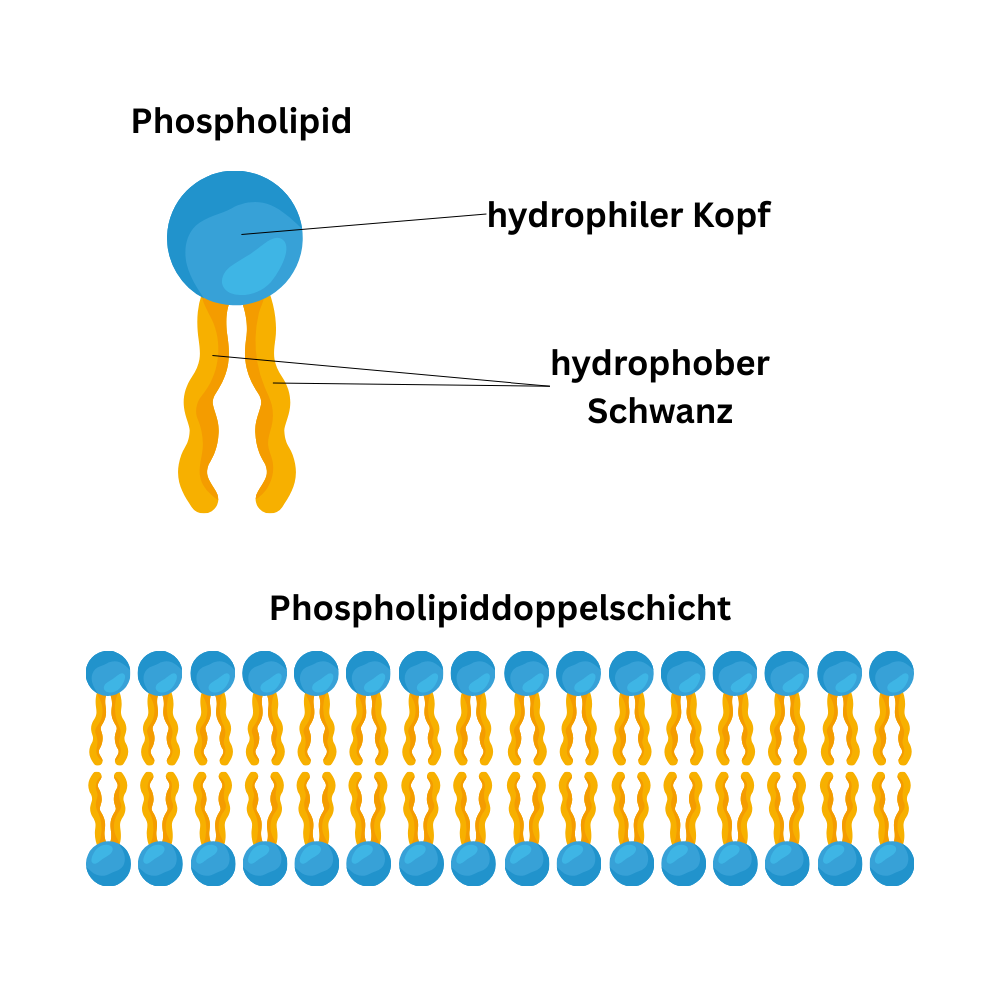
An Grenzflächen – etwa an einer Wasseroberfläche – ordnen sich Phospholipide deshalb regelmäßig an: Köpfe zum Wasser, Schwänze vom Wasser weg. In wässriger Umgebung können sich außerdem typische Aggregate bilden. Mizellen entstehen aus einer einzelnen Lipidschicht und bilden kugelige Strukturen mit einem lipophilen Inneren, wodurch fettlösliche Substanzen in einer wässrigen Umgebung „mitgenommen“ werden können. Vesikel bestehen dagegen aus einer Lipiddoppelschicht; sie schließen sich zu einer Kugel, sodass innen ein wässriger (hydrophiler) Hohlraum entsteht.
Nach demselben Prinzip ist auch die Zellmembran aufgebaut: Sie besteht aus einer Phospholipiddoppelschicht (Bilayer). Der hydrophobe Bereich liegt dabei im Inneren der Membran. Das hat eine direkte Konsequenz: Frei hindurch diffundieren können vor allem kleine, apolare Moleküle. Viele andere Stoffe (z. B. Ionen oder größere polare Moleküle) benötigen dagegen spezifische Transportwege. In diesem Sinn ist die Zellmembran semipermeabel.
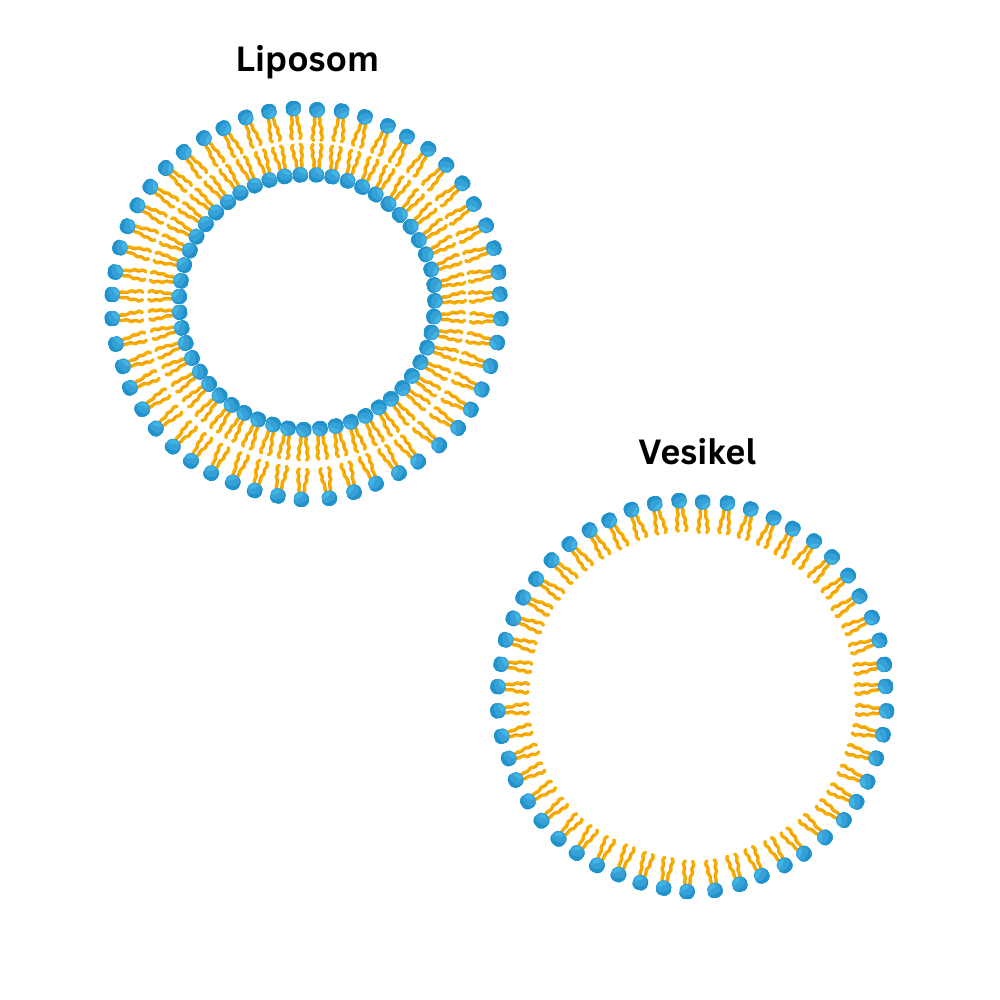
Die Doppelschicht ist nicht starr. Die hydrophoben Schwanzteile halten sich über relativ schwache hydrophobe Wechselwirkungen zusammen, wodurch die Lipide beweglich bleiben. Diese Beweglichkeit bezeichnet man als Fluidität der Membran. Häufig ist die laterale Diffusion (Phospholipide „wandern“ innerhalb derselben Schicht). Ein Wechsel von einer Membranseite zur anderen (transversale Diffusion, „Flip-Flop“) ist dagegen energetisch ungünstig und tritt deutlich seltener auf.
Ein entscheidender Regulator dieser Membraneigenschaften ist Cholesterin, das zwischen den Phospholipiden liegt. Bei höheren Temperaturen bremst es die Beweglichkeit und stabilisiert so die Membran. Bei niedrigeren Temperaturen verhindert es, dass die Membran zu starr wird, indem es eine zu dichte Packung der Lipide erschwert und damit die Flexibilität erhält.
Zusätzlich trägt die Zellmembran an ihrer Außenseite eine zuckerreiche Schicht: Die Oberfläche ist mit Glykolipiden und Glykoproteinen besetzt – zusammengefasst als Glykokalyx. Diese liegt immer extrazellulär und ist je nach Zelltyp und Organismus unterschiedlich. Funktionell ist sie besonders wichtig für Zell-Zell-Erkennung und -Interaktion, unter anderem im Rahmen immunologischer Unterscheidung zwischen „selbst“ und „fremd“.
Membranproteine
Neben den Lipiden prägen Membranproteine die Funktion der Zellmembran. Man unterscheidet grob integrale und periphere Membranproteine. Integrale Proteine sind in die Lipiddoppelschicht eingebettet und durchziehen sie häufig vollständig. Wenn sie die gesamte Membran durchspannen, spricht man von Transmembranproteinen. Solche Proteine können als Kanäle oder Transporter wirken und ermöglichen z. B. den Durchtritt von Ionen oder von Molekülen wie Glukose. Ein klassisches Beispiel sind Aquaporine, die als Wasserkanäle den kontrollierten Wasserdurchtritt ermöglichen.
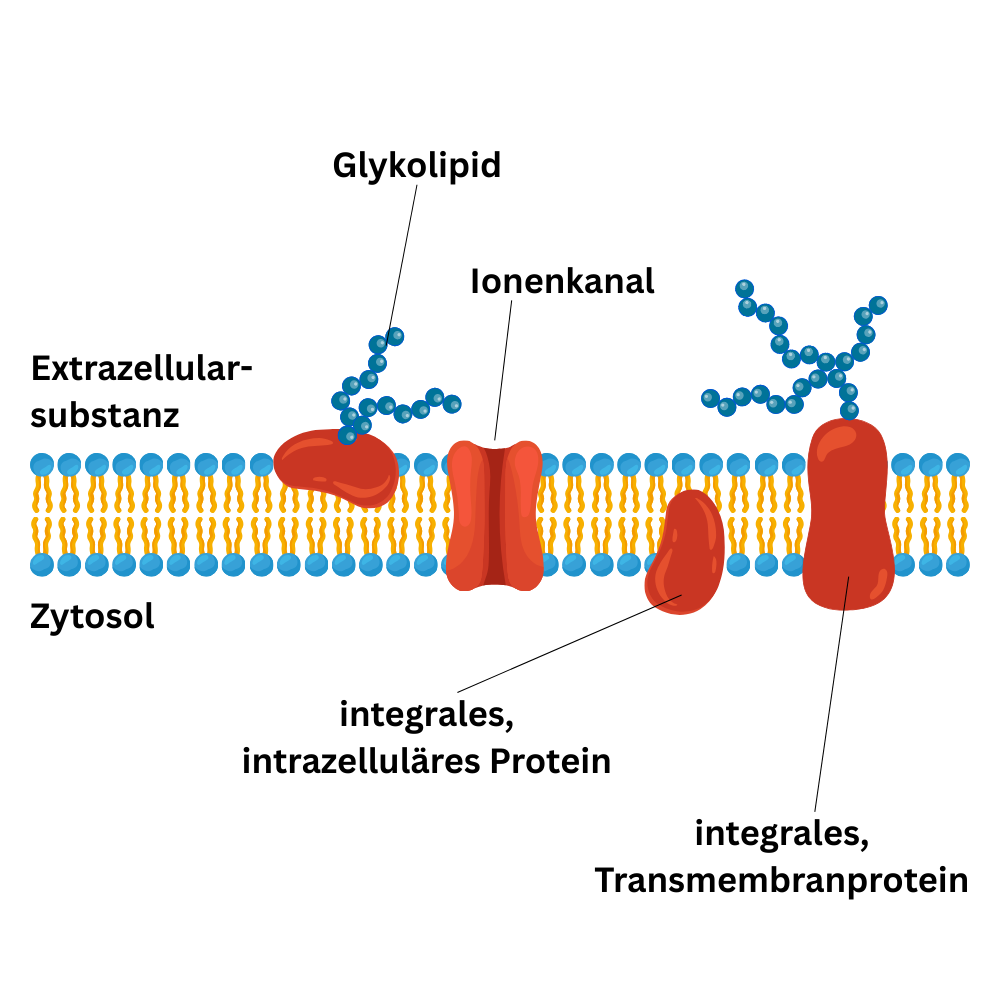
Periphere Membranproteine liegen dagegen nur an der Innen- oder Außenseite der Membran an. Sie übernehmen je nach Zelltyp unterschiedliche Aufgaben, etwa als Rezeptoren (teilweise mit Enzymaktivität) oder als Ankerpunkte zur Verbindung der Membran mit dem Zytoskelett.
Stofftransport
Damit eine Zelle funktionieren kann, muss sie ständig Stoffe mit ihrer Umgebung austauschen. An der Zellmembran geschieht dieser Austausch grundsätzlich auf zwei Wegen: entweder passiv (ohne direkten Energieverbrauch) oder aktiv (unter Energieaufwand). Welche Transportform möglich ist, hängt vor allem von Größe und Polarität/Lipophilie des Stoffes ab. Sehr kleine, unpolare Moleküle kommen oft schon durch einfache Diffusion durch die Lipiddoppelschicht. Kleine polare Teilchen oder Ionen benötigen dagegen Membranproteine. Größere Partikel werden meist über Vesikel aufgenommen oder abgegeben.
Ein zentrales Grundprinzip im Hintergrund ist die Diffusion: Teilchen bewegen sich aufgrund ihrer Eigenbewegung so, dass mit der Zeit eine möglichst gleichmäßige Verteilung entsteht. Der Motor ist dabei das Konzentrationsgefälle. Ein Sonderfall ist die Osmose. Hier diffundiert ein Lösungsmittel (in Zellen praktisch immer Wasser) durch eine semipermeable Membran in Richtung der Seite mit höherer Konzentration gelöster Teilchen, um den Unterschied im osmotischen Druck auszugleichen. Entscheidend ist dabei: Die gelösten Teilchen können die Membran nicht oder kaum passieren – deshalb „übernimmt“ Wasser die Bewegung.
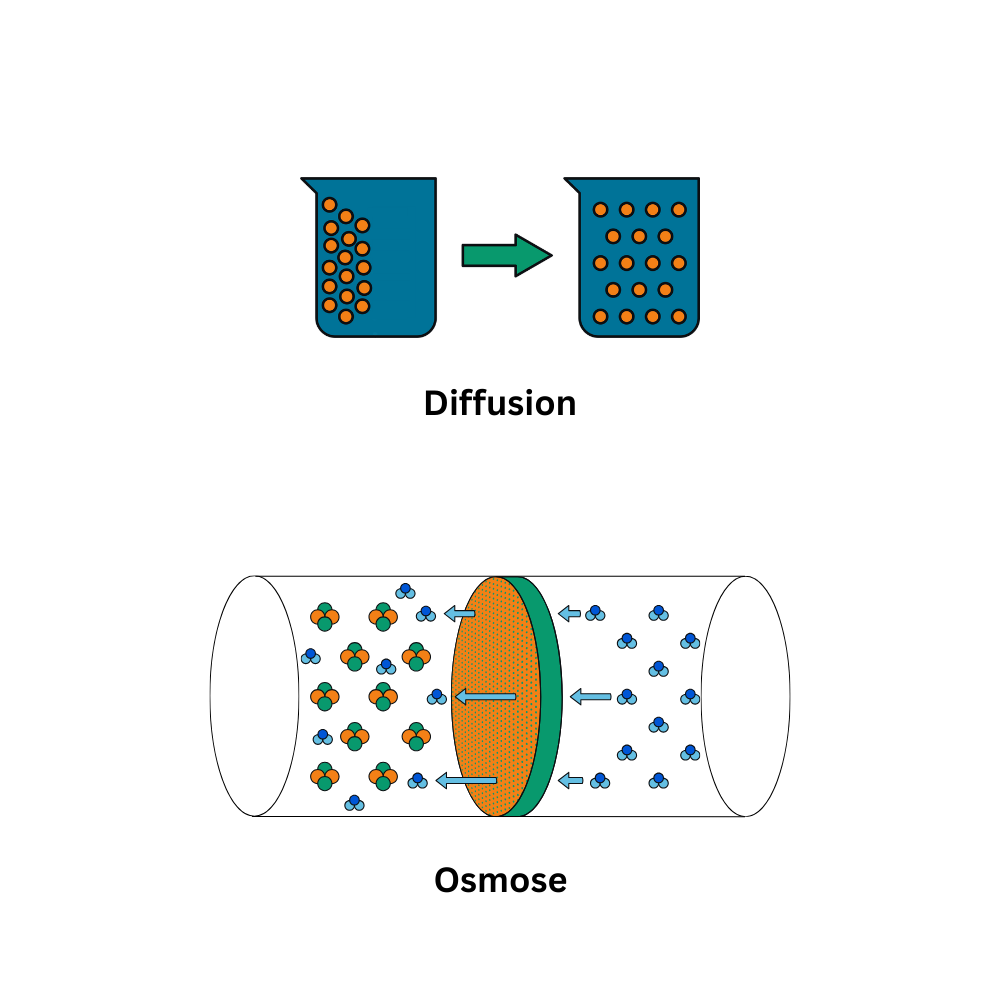
Passiver Transport
Beim passiven Transport werden Substanzen durch die Membran bewegt, ohne dass die Zelle dafür ATP einsetzen muss. Grundlage ist immer ein vorhandenes Gefälle (z. B. Konzentrationsgradient oder elektrochemischer Gradient).
Sehr kleine, lipophile Moleküle wie Sauerstoff (O₂) und Kohlenstoffdioxid (CO₂) können die lipophile Membran direkt durch einfache Diffusion durchqueren. Sie „wandern“ dabei von Bereichen hoher zu Bereichen niedriger Konzentration.
Hydrophile (lipophobe) Stoffe schaffen diesen Weg nicht durch die Lipidschicht. Für sie braucht es Transportproteine. Eine wichtige Gruppe sind Kanalproteine: Sie bilden Poren, durch die Teilchen entlang ihres Gradienten passieren können. Manche Kanäle sind konstitutiv offen, andere reguliert. So gibt es ligandengesteuerte Kanäle, die sich nach Bindung eines bestimmten Moleküls öffnen, und spannungsgesteuerte Kanäle, die auf Änderungen des Membranpotentials reagieren. Spezielle Kanäle sind Aquaporine, die den Wasserdurchtritt stark erleichtern, sowie typische Ionenkanäle (z. B. für Natrium- oder Kaliumionen).
Neben Kanälen gibt es Carrierproteine. Sie funktionieren anders: Ein Carrier bindet sein Substrat auf einer Membranseite, ändert dann seine räumliche Form (Konformationswechsel) und gibt das Molekül auf der anderen Seite wieder frei. Je nachdem, wie viele Stoffe bewegt werden und in welche Richtung, unterscheidet man Uniport (ein Stoff in eine Richtung), Symport (zwei Stoffe gemeinsam in dieselbe Richtung) und Antiport (zwei Stoffe gleichzeitig in entgegengesetzte Richtungen).
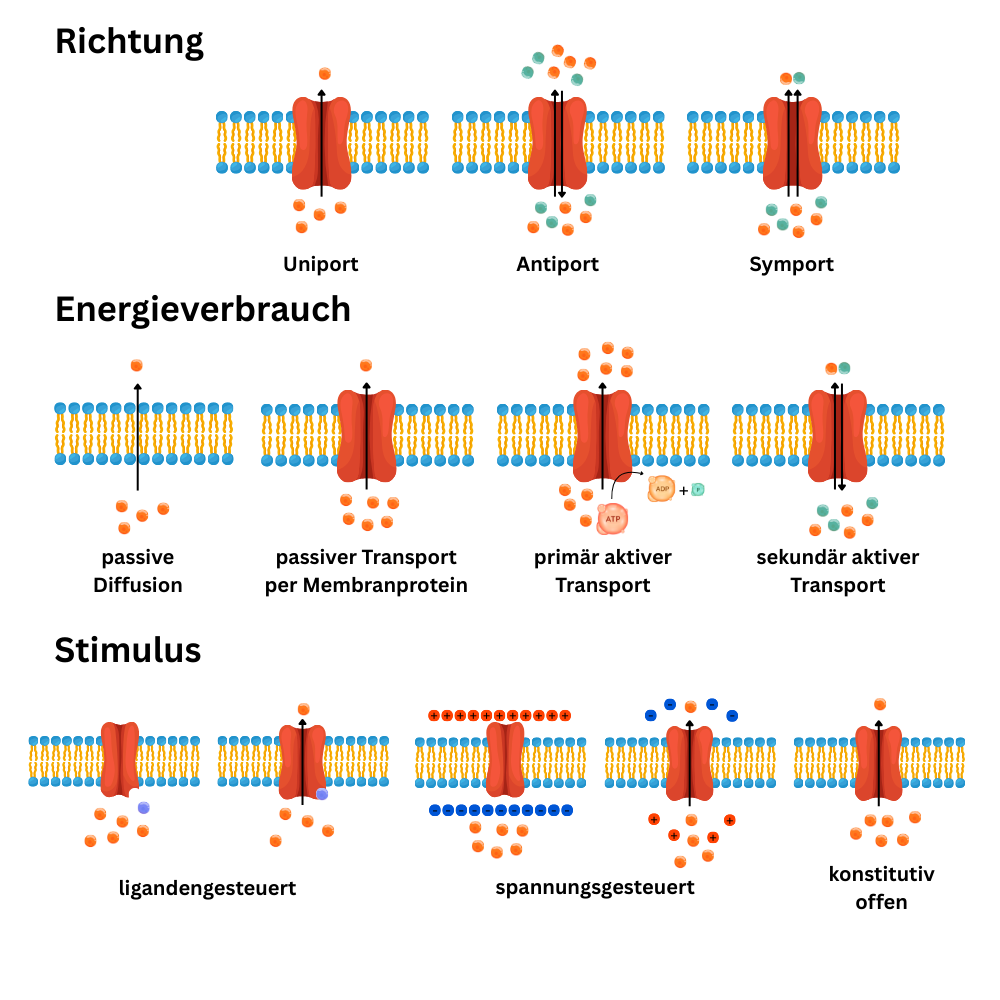
Aktiver Transport
Beim aktiven Transport werden Stoffe gegen ihr Gefälle durch die Membran transportiert. Das ist energetisch ungünstig und braucht daher Energie – in Zellen typischerweise in Form von ATP (Adenosintriphosphat). ATP ist der zentrale Energieträger: Ohne seine energiereichen Phosphatbindungen laufen die meisten energieverbrauchenden Prozesse der Zelle nicht mehr ausreichend ab.
Man unterscheidet zwei Grundformen. Beim primär aktiven Transport wird ATP direkt genutzt, um Ionen oder Moleküle gegen ihren Gradienten zu pumpen. Ein klassisches Beispiel ist die Natrium-Kalium-ATPase, die unter ATP-Verbrauch Natrium und Kalium in entgegengesetzte Richtungen transportiert und dadurch wichtige Ionengradienten aufrechterhält.
Beim sekundär aktiven Transport wird ATP nicht direkt am eigentlichen Transporter gespalten. Stattdessen nutzt die Zelle ein bereits vorhandenes Gefälle (meist eines Ions), das zuvor durch primär aktiven Transport aufgebaut wurde. Die „Energie“ dieses Gradienten treibt dann den Transport eines zweiten Stoffes mit an. Ein typisches Beispiel ist der Natrium-Glukose-Symporter: Das starke Natriumgefälle (außen mehr Natrium als innen) ermöglicht, dass Glukose zusammen mit Natrium in die Zelle aufgenommen werden kann – auch dann, wenn Glukose dabei gegen ihr eigenes Konzentrationsgefälle transportiert werden muss.
Exo- und Endozytose
Sehr große Moleküle oder Partikel können weder durch Diffusion noch über Kanäle oder Carrier effizient die Membran passieren. In solchen Fällen arbeitet die Zelle mit Vesikeln. Dieses vesikuläre „Ein- und Ausschleusen“ wird zusammengefasst als Zytose.
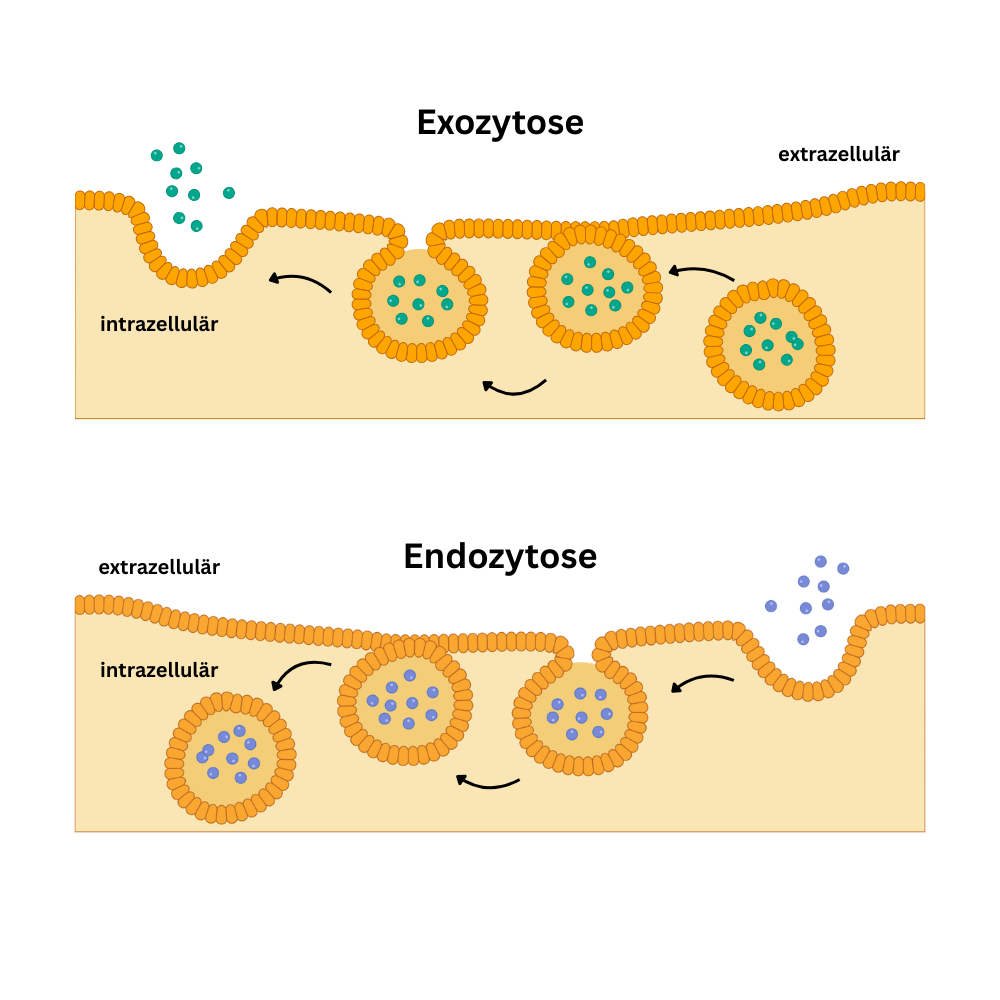
Bei der Endozytose nimmt die Zelle Material aus der Umgebung auf. Dazu stülpt sich die Zellmembran ein, schnürt ein Vesikel ab und bringt es ins Zellinnere. Eine Form davon ist die Pinozytose („trinken“): Hier werden Flüssigkeit und darin gelöste Stoffe in kleinen Vesikeln aufgenommen. Eine andere Form ist die Phagozytose („fressen“): Dabei werden größere Partikel wie Bakterien oder Zelltrümmer umschlossen. Es entsteht ein Phagosom, das anschließend mit Lysosomen fusioniert, sodass lysosomale Enzyme den Inhalt abbauen.
Bei der Exozytose ist die Richtung umgekehrt: Substanzen werden aus der Zelle abgegeben, indem Vesikel mit der Zellmembran fusionieren und ihren Inhalt nach außen freisetzen. Häufig werden die abzugebenden Moleküle zuvor im Golgi-Apparat in Vesikel verpackt. Durch die Fusion wird nicht nur Inhalt ausgeschleust, sondern gleichzeitig Membranmaterial eingebaut – Endo- und Exozytose sind daher immer auch mit einem fortlaufenden Umbau der Zellmembran verbunden.
Extrazellularraum #
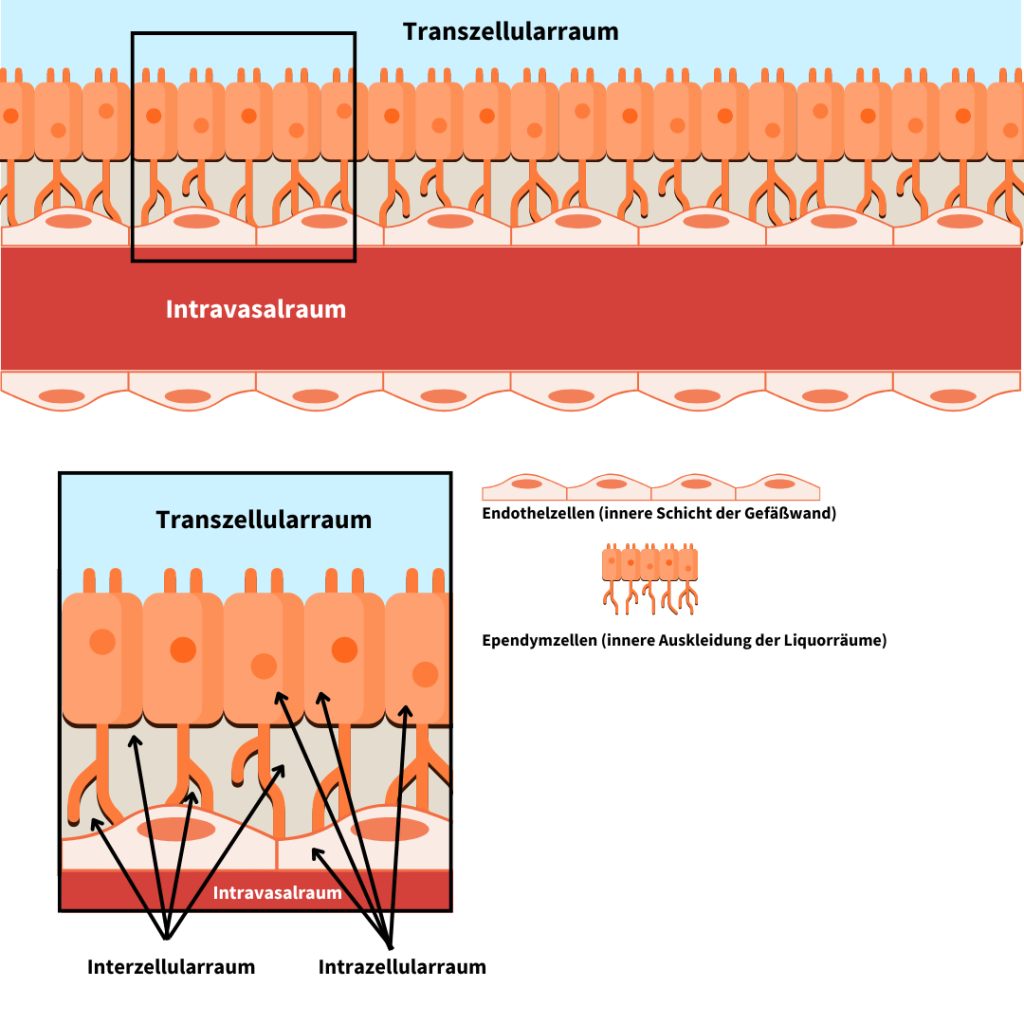
Der Extrazellularraum umfasst alles, was außerhalb der Zellen liegt, aber innerhalb eines Organismus. Praktisch ist das die „Flüssigkeits- und Stütz-Umgebung“, in die Zellen eingebettet sind. Zur Orientierung kann man den Extrazellularraum in drei Bereiche gliedern: den Intravasalraum (innerhalb von Blut- und Lymphgefäßen sowie den Herzhöhlen) und den Extravasalraum (außerhalb der Gefäße). Der Extravasalraum lässt sich wiederum in Interzellularraum und Transzellularraum unterteilen.
Der Transzellularraum meint flüssigkeitsgefüllte Hohlräume, die mit Epithel ausgekleidet sind (also „abgegrenzte“ Körperräume), während der Interzellularraum der Teil ist, der für das Zell- und Gewebeverständnis am wichtigsten ist: das ist der Raum zwischen benachbarten Zellen.
Interzellularraum
Der Interzellularraum ist nicht einfach „leer“. Er ist im Wesentlichen mit zwei Komponenten gefüllt: der Interzellularsubstanz (auch extrazelluläre Matrix, EZM) und der Interzellularflüssigkeit (auch interstitielle Flüssigkeit).
Die extrazelluläre Matrix (EZM) ist ein dreidimensionales Netzwerk aus Makromolekülen. Das ist keine zufällige Ablagerung, sondern ein hochorganisiertes Geflecht aus fadenförmigen Strukturen („Fasern“) und weiteren Matrixbestandteilen. Je nach Gewebe ist die Zusammensetzung unterschiedlich. Klassisch unterscheidet man kollagene, retikuläre und elastische Fasern. Das Verhältnis dieser Faserarten entscheidet wesentlich darüber, ob ein Gewebe eher fest/stabil oder eher beweglich/elastisch ist. Bestimmte Zellen sind außerdem über Hemidesmosomen (Zell–Matrix-Kontakte) in dieser Matrix verankert.
Die Interzellularflüssigkeit umspült die Matrix und die äußeren Anteile der Zellmembranen. Sie ist das Transportmedium für den Austausch von Nährstoffen, Sauerstoff und Stoffwechselprodukten zwischen den Zellen – also die „Arbeitsflüssigkeit“, über die Versorgung und Abtransport laufen. Gleichzeitig spielt sie eine zentrale Rolle für den Flüssigkeits- und Elektrolythaushalt. Im Durchschnitt besteht sie überwiegend aus Wasser (≈ 99 %), dazu kommen Elektrolyte (≈ 0,9 %) sowie sehr geringe Anteile an Glykosaminoglykanen, Proteoglykanen und Adhäsionsproteinen (jeweils typischerweise unter 0,1 %); je nach Gewebe können diese Anteile aber variieren.
Wie „groß“ der Interzellularraum wirkt, hängt stark vom Gewebe ab: In Epithelgeweben ist er oft nur ein schmaler Spalt (entsprechend spricht man auch vom Interzellularspalt). Im Bindegewebe dagegen ist er deutlich ausgeprägter und besteht aus Fasern (z. B. Kollagen, Elastin, Retikulin) plus Interzellularflüssigkeit; in diesem Kontext wird er auch als Grundsubstanz beschrieben.
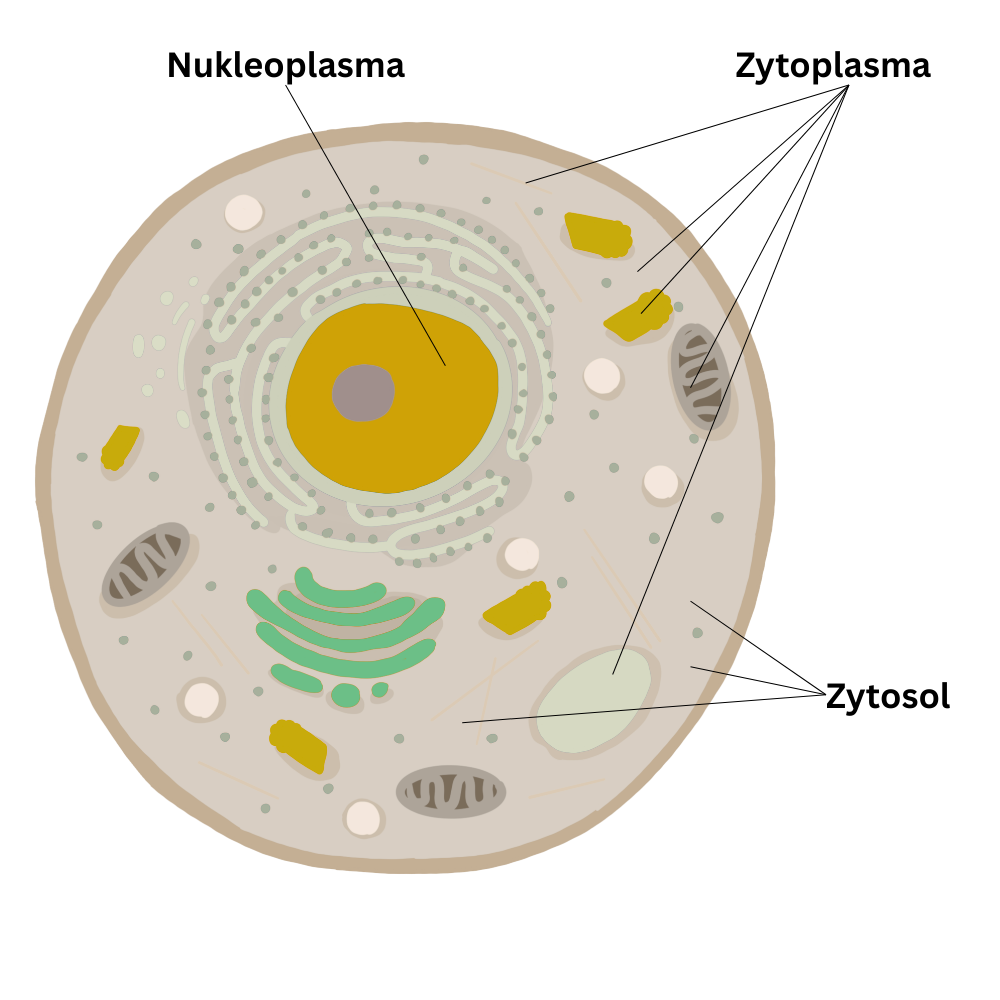
Protoplasma #
Als Protoplasma bezeichnet man den lebenden Zellinhalt, der vollständig von der Zellmembran umschlossen wird. Gemeint ist damit nicht einfach „Zellfüllung“, sondern die Gesamtheit der Bestandteile, die die Zellfunktionen ermöglichen. Praktisch lässt sich das Protoplasma in zwei große Bereiche gliedern: den Anteil im Zellkern (das Nukleoplasma/Karyoplasma) und den Anteil außerhalb des Zellkerns (das Zytoplasma).
Nukleoplasma
Das Nukleoplasma (auch Karyoplasma) ist die zähflüssig-gelartige Grundsubstanz im Inneren des Zellkerns. Es liegt innerhalb der Kernhülle, die den Zellkern als Doppelmembran umgibt. In diesem Kernraum befindet sich die genetische Information: Die DNA ist nicht frei im Raum verteilt, sondern zusammen mit Proteinen zu Chromatin organisiert. Zusätzlich finden sich im Nukleoplasma unter anderem RNA-Moleküle, Nukleotide sowie zahlreiche Enzyme, die für nukleäre Prozesse benötigt werden (z. B. Transkription, RNA-Verarbeitung und DNA-assoziierte Stoffwechselvorgänge).
Zytoplasma
Das Zytoplasma umfasst den lebenden Zellinhalt außerhalb des Zellkerns und ist ebenfalls durch die Zellmembran begrenzt. Funktionell setzt es sich aus dem Zytosol als wässriger Grundlösung, dem Zytoskelett als strukturgebendem Gerüst und – bei Eukaryoten – den Zellorganellen zusammen.
Das Zytosol ist keine „reine Wasserphase“, sondern eine komplexe Lösung, in der Proteine, Enzyme, Ionen und viele weitere Moleküle gelöst vorliegen. Mengenmäßig dominiert Wasser (grob im Bereich von 80–85 %), daneben machen Proteine typischerweise etwa 10–15 % aus. Kleinere Anteile entfallen auf Lipide (ca. 2–4 %) sowie weitere organische Moleküle und Mineralsalze (jeweils meist bis ~2 %). Zusätzlich finden sich geringe Mengen an Polysacchariden (bis etwa 1,5 %) sowie DNA/RNA (etwa ~1 %, je nach Zelltyp).
Das Zytoskelett ist das innere Stütz- und Organisationssystem der Zelle. Es besteht aus verschiedenen Proteinfilament-Netzwerken, die der Zelle Form geben, Kräfte abfangen, Transportprozesse ermöglichen und die räumliche Ordnung im Zellinneren mitbestimmen.
Wichtig ist: Das Zytoplasma ist nicht bloß „Material zwischen Organellen“, sondern der Ort, an dem ein großer Teil der zellulären Chemie abläuft. Außerdem findet hier – an freien Ribosomen – die Proteinbiosynthese für viele zytosolische Proteine statt. Zusätzlich erfüllt das Zytoplasma eine Speicherfunktion: Überschüssige Glukose kann hier als Glykogen abgelegt werden, besonders ausgeprägt in Leberzellen und Skelettmuskelzellen, damit bei Bedarf schnell Energie mobilisiert werden kann. Neben diesen gelösten und strukturierten Komponenten gibt es im Zytoplasma auch Einschlüsse, etwa Lipidtröpfchen oder Pigmentablagerungen (z. B. Melanin), die als Substanzdepots im Zellinneren liegen.
Zellkern #
Der Zellkern (Nukleus) ist das zentrale Steuer- und Informationszentrum der eukaryotischen Zelle. Er enthält im Karyoplasma den größten Teil der genetischen Information in Form von DNA. Diese DNA liegt nicht „frei“ vor, sondern ist zu Chromosomen organisiert und an Proteine – vor allem Histone – gebunden. Die Gesamtheit aus DNA und zugehörigen Proteinen nennt man Chromatin.
Chromatin kann unterschiedlich dicht gepackt sein. Euchromatin ist eher locker organisiert und damit gut zugänglich, wenn Gene abgelesen werden müssen. Heterochromatin ist dagegen stärker kondensiert und in der Regel weniger transkriptionsaktiv. Wichtig ist: Diese Zustände sind nicht starr, sondern können sich je nach Zelltyp, Aktivität und Phase des Zellzyklus verändern.
Nach außen wird der Zellkern durch die Kernhülle begrenzt, eine Doppelmembran mit einem schmalen Zwischenraum. Die äußere Kernmembran steht in direkter Verbindung mit dem endoplasmatischen Retikulum. An der Innenseite der Kernhülle liegt die Kernlamina, ein stabilisierendes Proteinnetzwerk. Sie gibt dem Zellkern Form und mechanische Festigkeit und dient außerdem als organisatorischer „Anker“ für Chromatin.
In die Kernhülle sind zahlreiche Kernporen eingebaut. Über diese Poren läuft der kontrollierte Austausch zwischen Zellkern und Zytoplasma: Kleine Moleküle können relativ leicht passieren, größere (z. B. Proteine oder RNA-Komplexe) werden gezielt transportiert.
Funktionell ist der Zellkern vor allem der Ort der DNA-Replikation (Verdopplung des Erbmaterials) und der Transkription, also der Umschreibung von DNA in RNA. Die daraus entstehende mRNA wird durch Kernporen ins Zytoplasma exportiert und dort – über Ribosomen, häufig am rauen ER – in Proteine übersetzt. Neben mRNA existieren weitere RNA-Formen mit spezifischen Aufgaben, zum Beispiel tRNA und rRNA.
Nicht alle Zelltypen besitzen einen Zellkern: reife Erythrozyten sind kernlos, und Thrombozyten enthalten ebenfalls keinen Zellkern (sie sind funktionell Zellfragmente aus Megakaryozyten).
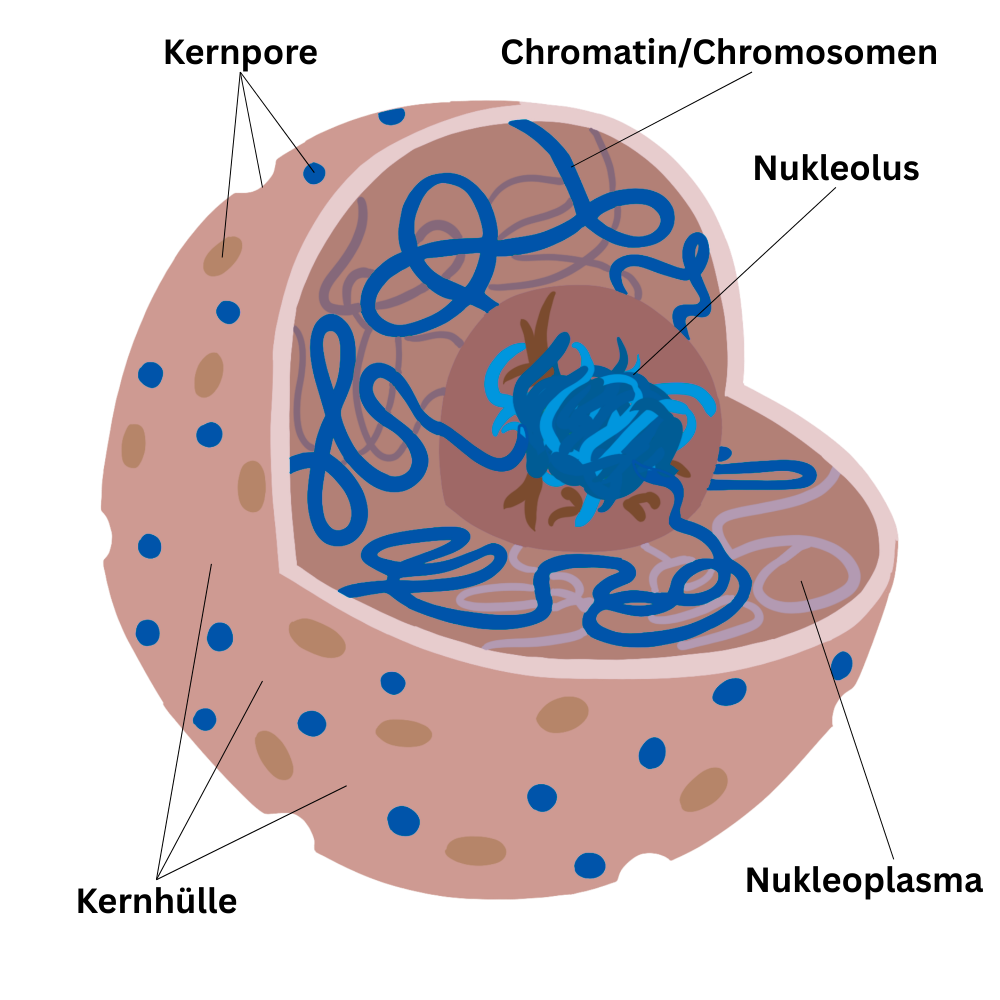
Nukleolus
Der Nukleolus (Kernkörperchen) ist eine gut erkennbare Struktur innerhalb des Zellkerns. Er ist kein eigenes membranumhülltes Organell, sondern eine funktionelle Kernregion, in der vor allem ribosomale RNA (rRNA) gebildet wird und die frühen Schritte der Ribosomenbiogenese stattfinden.
Beim Menschen hängt der Nukleolus mit speziellen DNA-Abschnitten zusammen, den Nucleolus Organizer Regions (NOR). Diese liegen auf bestimmten Chromosomen, nämlich 13, 14, 15, 21 und 22, und liefern die genetische Vorlage für die rRNA-Produktion.
Endoplasmatisches Retikulum und Ribosomen #
Das endoplasmatische Retikulum (ER) und die Ribosomen gehören funktionell eng zusammen, weil hier ein Großteil der Proteinbiosynthese organisiert und weiterverarbeitet wird. Das ER bildet dabei ein weit verzweigtes Membransystem im Zytoplasma eukaryotischer Zellen, das aus Kanälen und Zisternen besteht und einen eigenen Innenraum (ER-Lumen) abgrenzt. In der Zelle gibt es zwei Ausprägungen dieses Systems: ein raues und ein glattes ER.
Unabhängig von der jeweiligen Spezialisierung erfüllen beide ER-Formen eine gemeinsame Grundaufgabe: Durch die Bildung von Kompartimenten schafft das ER räumlich getrennte Reaktionsräume. Dadurch können bestimmte Stoffe lokal „gebündelt“ werden, was Reaktionen begünstigt und Stoffwechselprozesse effizienter macht.

Endoplasmatisches Retikulum
Beim rauen endoplasmatischen Retikulum (rER) fällt vor allem auf, dass seine dem Zytoplasma zugewandte Oberfläche dicht mit Ribosomen besetzt ist. Diese „Bepunktung“ erklärt das raue Erscheinungsbild im Mikroskop. Funktionell ist das rER der zentrale Ort, an dem Proteine synthetisiert werden, die anschließend weiterverarbeitet oder gezielt an bestimmte Orte gebracht werden müssen.
Direkt im Anschluss an die Synthese laufen im rER häufig posttranslationale Modifikationen ab. Darunter versteht man chemische Veränderungen an einem Protein nach der Translation, die seine Funktion, Stabilität oder seinen Zielort beeinflussen. Typische Beispiele sind die Glykosylierung (Anheften von Zuckerketten zur Stabilisierung und „Adressierung“), die Hydroxylierung (Einbau von Hydroxylgruppen, was u. a. Festigkeit und Löslichkeit verbessern kann) sowie die Bildung von Disulfidbrücken, die die dreidimensionale Struktur durch Bindungen zwischen Cysteinresten stabilisieren.
Das glatte endoplasmatische Retikulum (gER) trägt keine Ribosomen und wirkt daher „glatt“. Seine Aufgaben sind breit gefächert. Besonders wichtig ist die Synthese von Membranlipiden sowie die Bildung von Steroidhormonen (z. B. Testosteron und Östrogen). Deshalb findet man viel glattes ER in steroidproduzierenden Geweben wie Hoden, Ovarien und der Nebennierenrinde. In Muskelzellen übernimmt das gER außerdem eine Spezialrolle als Calciumspeicher; in diesem Kontext spricht man vom sarkoplasmatischen Retikulum. Die kontrollierte Freisetzung von Calcium ins Zytosol ist dabei ein entscheidender Schritt zur Auslösung der Muskelkontraktion.
In Leberzellen ist das gER ein zentrales Organell der Biotransformation: Es wandelt vor allem lipophile Substanzen (z. B. bestimmte Medikamente oder Gifte) in hydrophilere Formen um, damit sie leichter über Niere oder Galle ausgeschieden werden können. Zusätzlich ist das gER in den Kohlenhydratstoffwechsel eingebunden, unter anderem über die Glucose-6-Phosphatase, die aus Glucose-6-phosphat durch Abspaltung der Phosphatgruppe freie Glucose erzeugt, welche anschließend ins Blut abgegeben werden kann. Schließlich werden Stoffe häufig in Vesikel verpackt und zum Golgi-Apparat weitertransportiert, wo Modifikation, Sortierung und Versand an den endgültigen Bestimmungsort erfolgen.

Ribosomen
Ribosomen sind große makromolekulare Komplexe aus Proteinen und ribosomaler RNA (rRNA). Ihre Hauptaufgabe ist die Translation, also die Übersetzung der mRNA in eine Aminosäurekette, aus der später ein Protein entsteht. Ein eukaryotisches Ribosom besteht aus einer kleinen und einer großen Untereinheit, die nur dann zusammenkommen, wenn aktiv translatiert wird; in Ruhe liegen beide Untereinheiten getrennt im Zytoplasma vor.
Als Peptid bezeichnet man Aminosäureketten mit bis zu etwa 100 Aminosäuren; längere Ketten werden üblicherweise als Proteine bezeichnet. Die Verknüpfung der Aminosäuren erfolgt über die Peptidbindung, wobei bei der Bindungsbildung Wasser (H₂O) abgespalten wird. Funktionell übernimmt die kleine Untereinheit (bei Eukaryoten 40S) das „Ablesen“ der mRNA und das korrekte Positionieren auf der Vorlage. Die große Untereinheit (bei Eukaryoten 60S) katalysiert die eigentliche Verknüpfung der Aminosäuren zu einer wachsenden Kette. Zusammen ergibt das das 80S-Ribosom der Eukaryoten. In Bakterien, Mitochondrien und Chloroplasten finden sich dagegen 70S-Ribosomen, aufgebaut aus 30S– und 50S-Untereinheit.
Ribosomen kommen entweder frei im Zytoplasma vor oder sind an das raue ER gebunden. Freie Ribosomen synthetisieren vor allem Proteine, die im Zytoplasma verbleiben. Ribosomen am rER produzieren dagegen Proteine, die exportiert werden, in die Zellmembran eingebaut werden oder in Richtung Lysosomen weitergeleitet werden.
Das „S“ in 80S bzw. 70S steht für Svedberg und beschreibt die Sedimentationskonstante, also wie schnell ein Partikel bei Zentrifugation sedimentiert. Diese Größe hängt nicht nur von der Masse, sondern auch von Form und Dichte ab – deshalb ist die Svedberg-Zahl nicht linear additiv (40S + 60S ergibt nicht 100S, sondern 80S).
Mehrere Ribosomen können gleichzeitig dieselbe mRNA bearbeiten. Solche Verbände nennt man Polysomen (Polyribosomen). Sie ermöglichen, dass aus einer einzigen mRNA parallel mehrere identische Polypeptidketten entstehen, wodurch die Proteinproduktion deutlich effizienter wird.

Golgi-Apparat #
Der Golgi-Apparat ist die zentrale Sortier-, Modifikations- und Versandstation der Zelle. Er übernimmt vor allem Proteine, die zuvor am rauen endoplasmatischen Retikulum hergestellt wurden, verarbeitet sie weiter und sorgt dafür, dass sie korrekt „verpackt“ und an ihren Zielort gebracht werden. Ein besonders wichtiger Punkt dabei ist, dass aus dem Golgi-Apparat auch Lysosomen hervorgehen.
Strukturell besteht der Golgi-Apparat aus mehreren flachen, membranumhüllten Hohlräumen, den Zisternen. Diese Zisternen sind zu Stapeln organisiert; solche Stapel werden als Dictyosomen bezeichnet. Der Golgi-Apparat besitzt dabei eine klare Polarität: Auf der dem ER zugewandten Seite liegt das cis-Golgi-Netzwerk, das die neu angelieferten Proteine aus dem ER aufnimmt. Auf der gegenüberliegenden Seite befindet sich das trans-Golgi-Netzwerk. Dort werden die fertig bearbeiteten Proteine in Vesikel abgeschnürt und anschließend zu ihrem endgültigen Bestimmungsort transportiert.
Im Golgi-Apparat laufen zahlreiche posttranslationale Modifikationen ab, die über Funktion, Stabilität und Zielsteuerung von Proteinen entscheiden. Ein zentraler Prozess ist die Glykosylierung, bei der Zuckerreste an Proteine angehängt werden, was ihre Stabilität erhöhen und ihre Erkennung durch andere Moleküle erleichtern kann. Außerdem werden im Golgi-Apparat Proteine markiert, die später in Lysosomen gelangen sollen. Zusätzlich können Peptidabschnitte abgespalten werden, um ein Protein in seine aktive Form zu überführen. Weitere typische Veränderungen sind die Sulfatierung (Anheften von Sulfatgruppen, SO₄²⁻) sowie die Phosphorylierung (Anheften von Phosphatgruppen, PO₄³⁻). Über solche Modifikationen kann die Zelle Aktivität und Signalverhalten der betroffenen Proteine gezielt beeinflussen.

Mitochondrium #
Viele Prozesse in der Zelle laufen nur dann ausreichend schnell ab, wenn sie von Enzymen katalysiert werden. Enzyme sind meist große Proteine, die chemische Reaktionen beschleunigen, ohne dabei selbst verbraucht zu werden. Häufig erkennt man Enzyme daran, dass ihre Namen auf -ase enden.
Mitochondrien sind die zentralen Organellen der Energiegewinnung. Sie stellen Adenosintriphosphat (ATP) her, also den universellen Energieträger, den Zellen für praktisch alle energieverbrauchenden Vorgänge benötigen. Weil ATP nur in sehr begrenztem Ausmaß gespeichert werden kann, kommen Mitochondrien in fast allen eukaryotischen Zellen vor, um Energie kontinuierlich bereitzustellen. Zellen mit besonders hohem Energiebedarf – etwa Herzmuskel- oder Nervenzellen – besitzen daher typischerweise besonders viele Mitochondrien. Reife Erythrozyten sind eine wichtige Ausnahme: Sie enthalten keine Mitochondrien (und auch keine anderen Organellen wie Zellkern oder Ribosomen). Dadurch können sie mehr Hämoglobin transportieren und verbrauchen selbst weniger Sauerstoff.
Strukturell sind Mitochondrien durch eine Doppelmembran gekennzeichnet. Diese umschließt die mitochondriale Matrix (Matrixraum). In der Matrix liegen zahlreiche Enzyme, außerdem mitochondriale DNA (mtDNA), Ribosomen und tRNAs. Die mtDNA wird beim Menschen mütterlich vererbt, da Mitochondrien aus dem Spermium bei der Befruchtung nicht in die Eizelle gelangen bzw. dort eliminiert werden. Auffällig ist zudem, dass mitochondriale Ribosomen 70S-Ribosomen sind – ein Hinweis auf den evolutiven Ursprung der Mitochondrien im Sinne der Endosymbiontentheorie. Mitochondrien können sich außerdem unabhängig vom Zellzyklus durch Teilung vermehren.
Zwischen äußerer und innerer Membran liegt der Intermembranraum. Die äußere Membran ist glatt, enthält – im Gegensatz zur inneren – Cholesterin und besitzt Porine (tunnelförmige Membranproteine). Dadurch ist sie für kleine Moleküle und Ionen relativ gut passierbar. Die innere Membran ist dagegen besonders spezialisiert: Sie enthält viel Cardiolipin (ein Phospholipid, das sonst in Zellen kaum vorkommt) und wenig bis gar kein Cholesterin. Außerdem ist sie stark gefaltet; diese Faltungen können je nach Zelltyp unterschiedlich ausgeprägt sein. In stoffwechselaktiven Geweben findet man häufig den Cristae-Typ mit flächigen, blattförmigen Einstülpungen (klassisch z. B. im Herzmuskel). In steroidproduzierenden Zellen (z. B. Nebennieren, Gonaden) ist eher ein Tubulus-Typ mit röhrenförmiger innerer Membran typisch. Seltener kommt ein Sacculus-Typ mit sackartigen Membranstrukturen vor (unter anderem in der Zona glomerulosa der Nebennierenrinde).
Funktionell ist die Kompartimentierung entscheidend: In der Matrix wird Acetyl-CoA im Citratzyklus zu CO₂ abgebaut; dabei entstehen die reduzierten Coenzyme NADH und FADH₂. Auch die β-Oxidation läuft in der Matrix ab und liefert zusätzlich Acetyl-CoA für den Citratzyklus. In der inneren Membran werden Elektronen aus NADH/FADH₂ über die Atmungskette weitergegeben. Dabei werden Protonen in den Intermembranraum gepumpt, wodurch ein Protonengradient entsteht. Dieser Gradient treibt die ATP-Synthase an, die aus ADP und Phosphat ATP bildet.
Neben der Energieproduktion haben Mitochondrien weitere zentrale Aufgaben. Sie sind an der Apoptose beteiligt, unter anderem über die Freisetzung von Cytochrom c aus dem Intermembranraum, was eine Signalkaskade zur kontrollierten Zerstörung der Zelle auslösen kann. Außerdem beeinflussen sie den Calciumhaushalt in der Matrix und damit zahlreiche Signalwege.
Die besondere Zusammensetzung der inneren Membran macht sie insgesamt wenig durchlässig für viele Ionen und Moleküle. Deshalb braucht die Zelle spezifische Transporter und Shuttle-Systeme, um Substrate in das Mitochondrium hinein- oder herauszubringen – ein Punkt, der auch erklärt, warum es häufig schwierig ist, Wirkstoffe gezielt in Mitochondrien zu bringen.

Lysosomen, Proteasomen und Peroxisomen #
Damit eine Zelle stabil funktioniert, muss sie ständig „aufräumen“: Defekte oder überflüssige Moleküle müssen abgebaut, gefährliche Zwischenprodukte entgiftet und bestimmte Stoffe gezielt recycelt werden. Dafür nutzt die Zelle verschiedene Abbau- und Entsorgungssysteme. Lysosomen übernehmen vor allem den Abbau von Material, das über Vesikel in die Zelle gelangt oder aus zelleigenen Bestandteilen stammt. Proteasomen sind dagegen auf den gezielten Abbau von Proteinen spezialisiert. Peroxisomen dienen vor allem der oxidativen Entgiftung und dem Abbau bestimmter Fettsäuren.
Lysosomen
Lysosomen sind membranumhüllte Organellen, die als „Verdauungseinheiten“ der Zelle funktionieren. Ihr Innenraum ist sauer, was entscheidend ist, weil dort zahlreiche saure Hydrolasen arbeiten. Diese Enzyme spalten große Biomoleküle wie Proteine, Lipide, Kohlenhydrate oder Nukleinsäuren in kleinere Bestandteile, die anschließend wiederverwendet oder weiter abgebaut werden können.
Die saure Umgebung entsteht, weil Protonen aktiv in das Lysosomeninnere gepumpt werden (typisch über protonentransportierende ATPasen). Dadurch sind die lysosomalen Enzyme im Lysosom optimal aktiv, während sie im neutraleren Zytosol deutlich weniger wirksam wären – das schützt die Zelle zusätzlich vor unkontrolliertem Abbau.
Lysosomen sind eng in den Vesikelverkehr eingebunden. Material kann von außen über Endozytose aufgenommen werden und gelangt über endosomale Zwischenstufen schließlich in lysosomale Abbaukompartimente. Ebenso kann die Zelle eigene Bestandteile über Autophagie in Vesikel verpacken und dem lysosomalen Abbau zuführen. Das ist wichtig, um beschädigte Organellen zu entfernen und in Zeiten von Nährstoffmangel Bausteine zurückzugewinnen.

Proteasomen
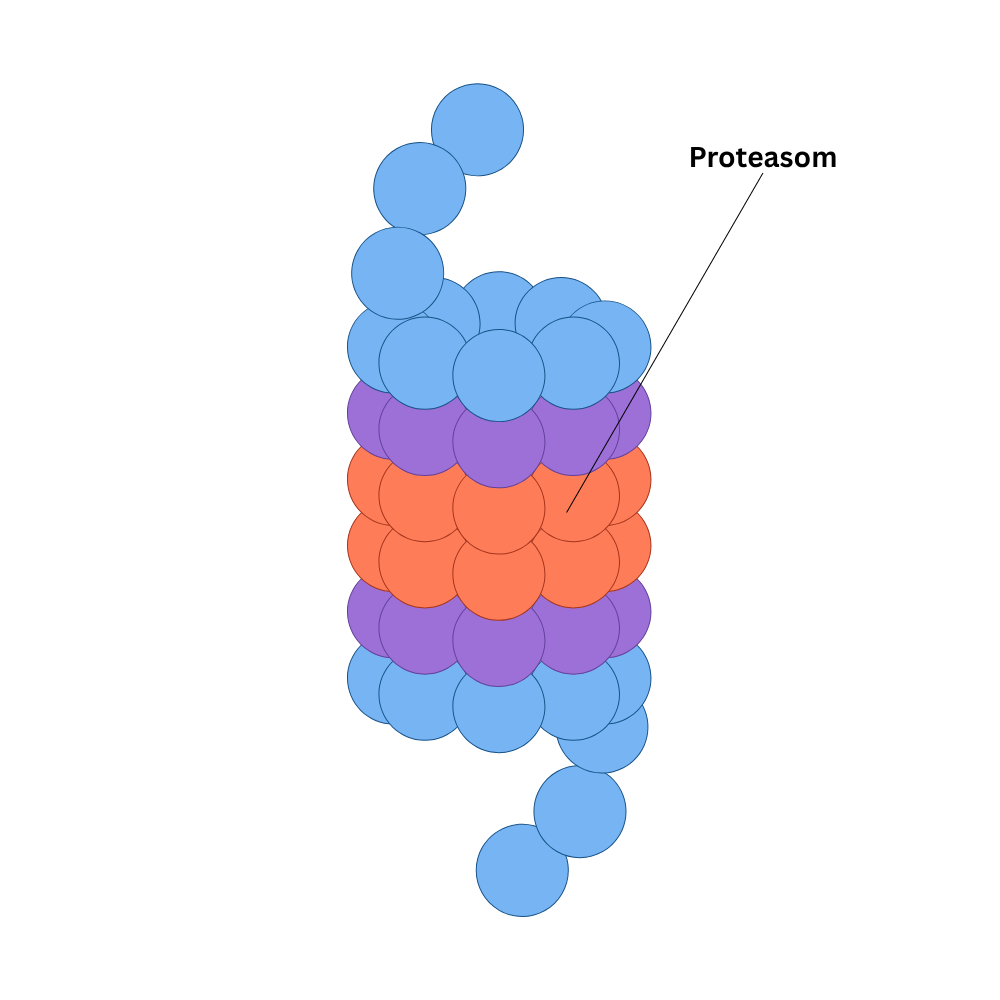
Während Lysosomen vor allem mit vesikulär angeliefertem Material arbeiten, ist das Proteasom das zentrale System für den gezielten Abbau zytosolischer und nukleärer Proteine. Proteine werden dabei nicht zufällig zerstört, sondern sehr selektiv. Der „Adressaufkleber“ für diesen Abbau ist meistens Ubiquitin: Proteine, die abgebaut werden sollen, werden mit Ubiquitin markiert. Diese Markierung signalisiert dem Proteasom, dass das Protein aufgenommen und zerlegt werden soll.
Das Proteasom selbst ist ein großer Proteinkomplex, der Proteine in kleinere Peptidstücke spaltet. Der Prozess ist für die Zelle enorm wichtig, weil so kurzlebige Regulationsproteine (z. B. aus dem Zellzyklus), falsch gefaltete Proteine oder durch Stress beschädigte Proteine entfernt werden. Damit ist das Proteasom ein Kernmechanismus der Qualitätskontrolle und der feinen Regulation zellulärer Prozesse.
Peroxisomen
Peroxisomen sind ebenfalls membranumhüllte Organellen, unterscheiden sich funktionell aber deutlich von Lysosomen. Ihr Schwerpunkt liegt auf oxidativen Reaktionen. Typisch ist die Bildung von Wasserstoffperoxid (H₂O₂) als Zwischenprodukt. Weil H₂O₂ zellschädigend sein kann, enthalten Peroxisomen besonders charakteristische Enzyme wie die Katalase, die H₂O₂ wieder zu Wasser und Sauerstoff abbaut. Dadurch werden potenziell gefährliche Oxidationsprodukte kontrolliert „entschärft“.
Ein weiterer zentraler Bereich ist der Fettstoffwechsel: Peroxisomen sind besonders wichtig für den Abbau bestimmter Fettsäuren, vor allem sehr langkettiger Fettsäuren, die nicht primär in Mitochondrien verarbeitet werden. Außerdem spielen Peroxisomen je nach Zelltyp eine Rolle bei der Synthese spezieller Lipide und bei Entgiftungsprozessen, besonders ausgeprägt in stoffwechselaktiven Geweben wie der Leber.
Peroxisomen besitzen keine eigene DNA. Sie vermehren sich typischerweise durch Wachstum und Teilung bereits vorhandener Peroxisomen, wobei Proteine aus dem Zytosol importiert werden.

Zytoskelett #
Das Zytoskelett ist das innere Stütz- und Organisationssystem der Zelle. Es sorgt dafür, dass Zellen ihre Form behalten, mechanische Belastungen abfangen und ihre Organellen räumlich geordnet bleiben. Gleichzeitig ist es ein dynamisches System: Es kann sich umbauen, Wachstum ermöglichen, die Zellbewegung steuern und während der Zellteilung die Verteilung der Chromosomen und die Trennung der Tochterzellen koordinieren. Funktionell ist das Zytoskelett außerdem die „Schieneninfrastruktur“ für den intrazellulären Transport: Vesikel und Organellen werden entlang von Filamenten durch Motorproteine zielgerichtet bewegt.
Grundsätzlich besteht es aus drei Filamentsystemen, die sich in Aufbau, Stabilität und Aufgaben unterscheiden: Mikrotubuli, Intermediärfilamente und Aktinfilamente. Diese Systeme arbeiten nicht isoliert, sondern sind über zahlreiche Bindungsproteine miteinander und mit der Zellmembran gekoppelt.
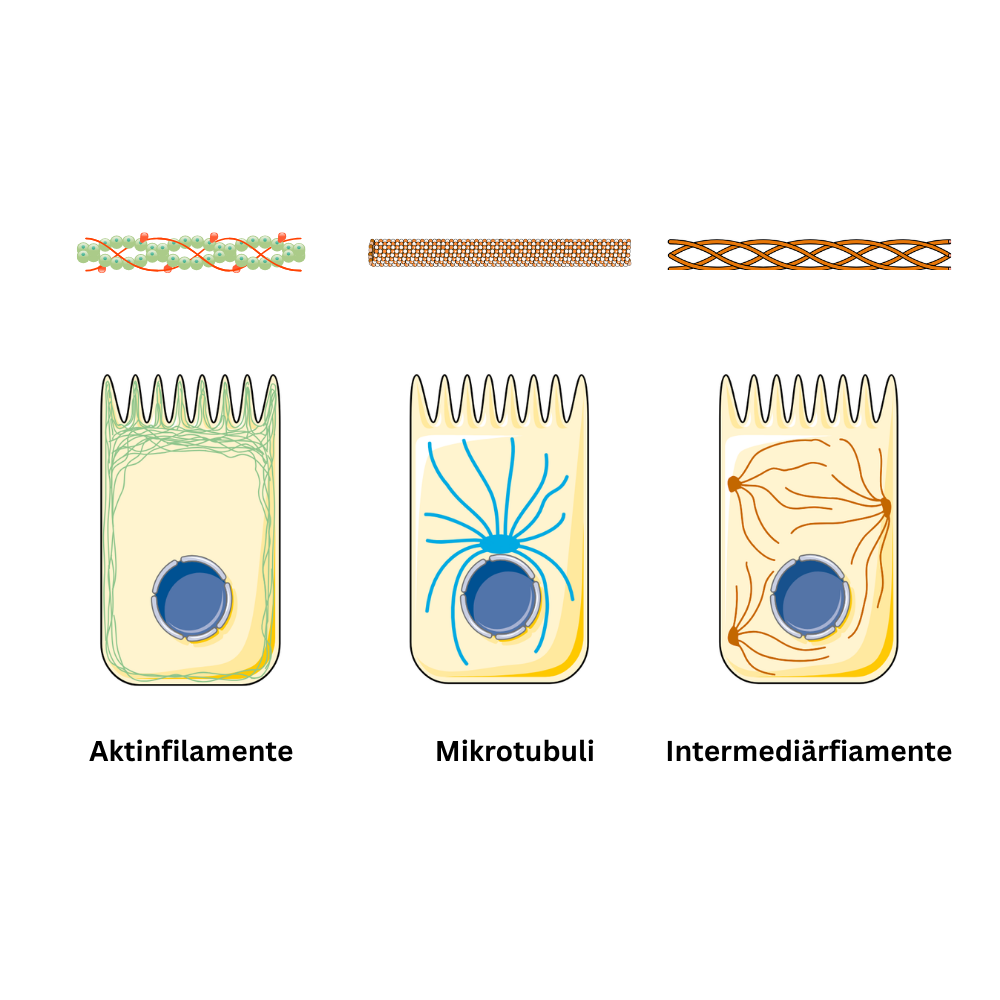
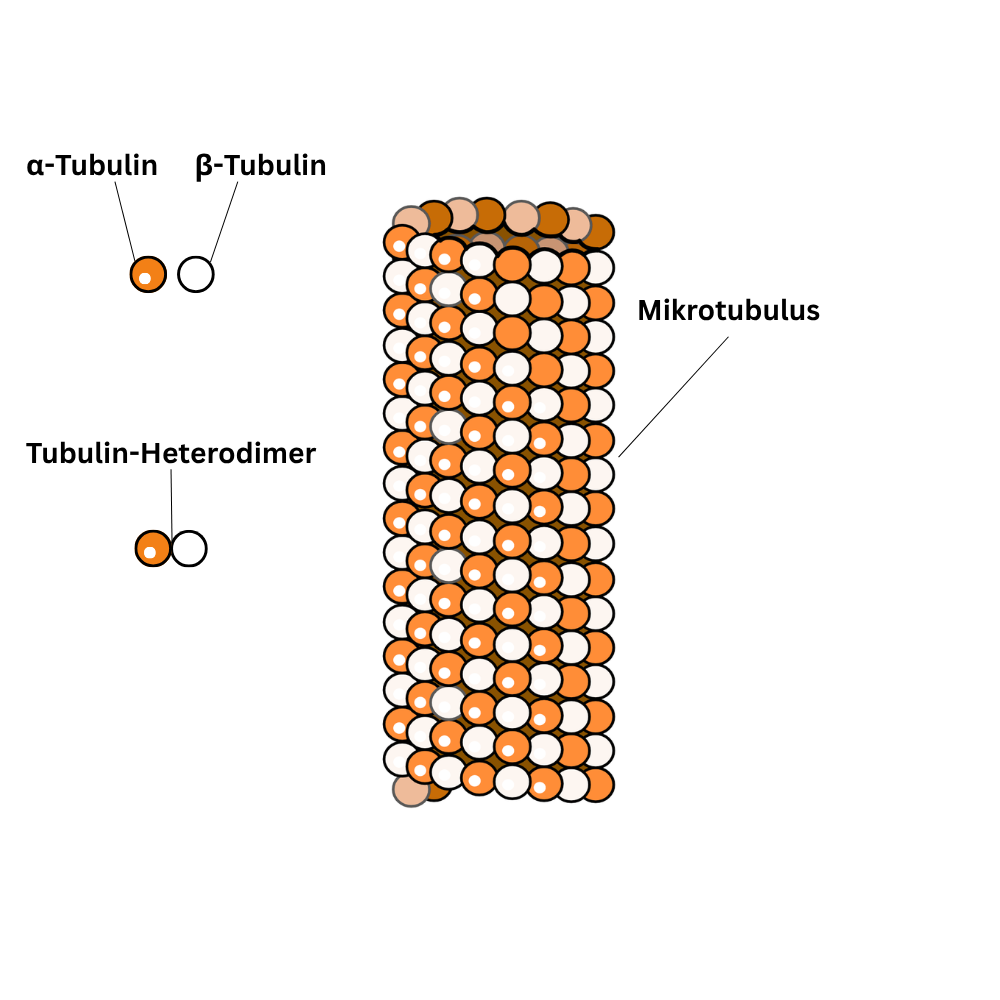
Mikrotubuli
Mikrotubuli sind röhrenförmige Strukturen, die aus dem Protein Tubulin aufgebaut werden. Genauer lagern sich α- und β-Tubulin zu Dimeren zusammen, aus denen längliche Protofilamente entstehen; mehrere Protofilamente bilden dann die typische „Röhre“. Mikrotubuli besitzen eine Polarität (ein Plus- und ein Minus-Ende). Das ist wichtig, weil Wachstum und Abbau bevorzugt an bestimmten Enden stattfinden und weil Motorproteine diese Polarität „lesen“.
Mikrotubuli sind besonders dynamisch: Sie können rasch wachsen und ebenso rasch wieder zerfallen. Dieses Verhalten ist zentral, wenn die Zelle ihre Form anpasst, Material transportiert oder sich teilt. Im Zellinneren gehen Mikrotubuli häufig von einem Organisationszentrum aus, dem Centrosom, und strahlen von dort in das Zytoplasma aus. Als Transportbahnen ermöglichen sie den gerichteten Vesikel- und Organellentransport, beispielsweise in Nervenzellen über sehr lange Strecken entlang der Axone. Die Bewegung wird durch Motorproteine vermittelt, vor allem durch Kinesin und Dynein, die „Fracht“ in definierte Richtungen entlang der Mikrotubuli ziehen.
In der Zellteilung sind Mikrotubuli unverzichtbar, weil sie den Spindelapparat bilden. Über diesen wird das Erbgut geordnet erfasst, ausgerichtet und schließlich auf die beiden Tochterzellen verteilt.
Zentriolen
Zentriolen sind spezielle, zylindrische Strukturen, die eng mit dem Mikrotubuli-System verbunden sind. Typischerweise liegen sie paarig im Centrosom und sind dort in ein perizentrioläres Material eingebettet, das als Ausgangspunkt für Mikrotubuli dient. Charakteristisch ist ihr Aufbau aus neun Mikrotubuli-Tripletts, die ringförmig angeordnet sind.
Während der Zellteilung spielt das Centrosom mit seinen Zentriolen eine zentrale Rolle beim Aufbau des Spindelapparats. Zentriolen können sich zudem in Basalkörperchen umwandeln und dann als „Anker“ für Kinozilien oder Geißeln dienen, also für bewegliche oder oberflächenvergrößernde Zellfortsätze. Wichtig ist auch, dass Zentriolen im Zellzyklus kontrolliert dupliziert werden, damit jede Tochterzelle wieder ein funktionsfähiges Organisationszentrum besitzt.
Intermediärfilamente
Intermediärfilamente sind vor allem für mechanische Stabilität zuständig. Im Gegensatz zu Mikrotubuli und Aktinfilamenten sind sie weniger dynamisch und besitzen keine ausgeprägte Polarität. Dadurch eignen sie sich besonders gut, um Zug- und Scherkräfte in der Zelle zu verteilen und Gewebe belastbar zu machen.
Intermediärfilamente sind je nach Zelltyp unterschiedlich zusammengesetzt. In Epithelzellen dominieren Keratine, im Bindegewebe findet man typischerweise Vimentin, in Muskelzellen Desmin, in Nervenzellen Neurofilamente. Eine Sonderform sind die Lamine, die als Netz an der Innenseite der Kernhülle liegen und so die Kernform stabilisieren. Intermediärfilamente sind außerdem eng an Zellkontakte gekoppelt: Sie verankern sich beispielsweise an Desmosomen (Zell–Zell-Verbindungen) und Hemidesmosomen (Zell–Matrix-Verbindungen) und tragen so wesentlich zur Gewebefestigkeit bei.

Aktinfilamente
Aktinfilamente (Mikrofilamente) bestehen aus Aktin und sind besonders wichtig für Formänderungen, Zellbewegung und Kraftentwicklung. Auch sie besitzen eine Polarität und können sich schnell auf- und abbauen. Ein großer Anteil der Aktinfilamente liegt direkt unter der Zellmembran als Zellkortex. Dieser Bereich bestimmt wesentlich, wie stabil oder flexibel die Zelloberfläche ist und wie gut die Zelle ihre Form aktiv verändern kann.
Aktinfilamente ermöglichen unterschiedliche Arten von Bewegung: Zellen können Fortsätze ausbilden, sich über Oberflächen vorwärts bewegen und ihre Membran dynamisch umorganisieren. In vielen Zellen sind Aktinstrukturen außerdem für Oberflächenvergrößerungen wichtig, beispielsweise in Mikrovilli. In Muskelzellen bildet Aktin zusammen mit Myosin den zentralen Apparat für die Kontraktion. Auch bei der Zellteilung ist Aktin entscheidend: Bei der Cytokinese entsteht ein kontraktiler Ring aus Aktin und Myosin, der die Zelle am Ende in zwei Tochterzellen abschnürt.
Insgesamt ist das Zytoskelett damit nicht nur ein „Gerüst“, sondern ein hochaktives System, das Stabilität, Transport, Bewegung und Zellteilung in einer funktionellen Einheit verbindet.

Kinozilien, Geisseln, Mikrovilli #
Die Zellmembran kann unterschiedliche Fortsätze/Ausstülpungen bilden, die der Zelle zusätzliche Funktionen geben. Dazu zählen Kinozilien, Geißeln und Mikrovilli. Gemeinsam ist ihnen, dass sie aus Elementen des Zytoskeletts aufgebaut sind. Je nach Typ dienen sie vor allem der Bewegung, dem Transport von Flüssigkeiten an der Zelloberfläche oder der Oberflächenvergrößerung.
Kinozilien
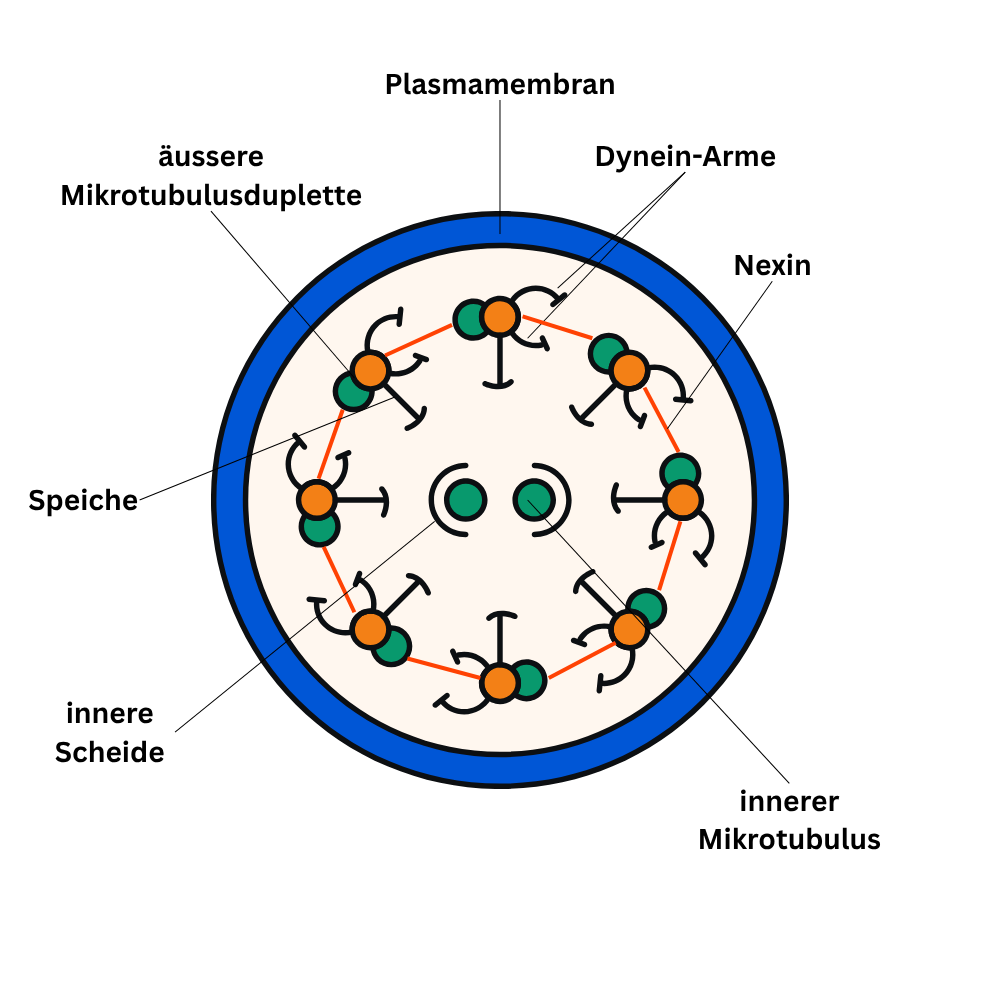
Kinozilien (Zilien) sind haarähnliche, aktiv bewegliche Zellfortsätze. Ihr Grundgerüst besteht aus Mikrotubuli und folgt einem typischen Bauplan, der als 9 × 2 + 2-Struktur beschrieben wird: Neun äußere Mikrotubulus-Dupletten liegen ringförmig um zwei zentrale einzelne Mikrotubuli. Jede Duplette setzt sich aus einem vollständigen A-Tubulus (mit 13 Protofilamenten) und einem unvollständigen B-Tubulus (mit 10 Protofilamenten) zusammen.
Die Bewegung entsteht durch Dynein-Arme, die an den äußeren Dupletten sitzen. Dynein wirkt als Motorprotein und verschiebt Mikrotubuli unter ATP-Verbrauch gegeneinander. Damit diese Verschiebung nicht einfach in ein unkontrolliertes „Gleiten“ übergeht, sind die Dupletten über Nexin-Verbindungen miteinander gekoppelt. Dadurch wird das Gleiten mechanisch begrenzt und in eine koordinierte Biegung umgewandelt. Zusätzlich stabilisieren (Radial-)Speichen die äußeren Dupletten, indem sie sie mit den zentralen Mikrotubuli verbinden – das sorgt für eine funktionell abgestimmte Schlagbewegung.
Funktionell erzeugen Kinozilien durch ihren koordinierten Schlag einen Flüssigkeitsstrom an der Zelloberfläche. In den Atemwegen transportieren sie Schleim mit eingeschlossenen Partikeln Richtung Rachen, wo er abgehustet oder geschluckt werden kann. Im Eileiter unterstützen sie den Transport der Eizelle in Richtung Gebärmutter.
Geißeln
Geißeln (Flagellen) sind lange, peitschenartige Fortsätze, die der Fortbewegung einer Zelle dienen. Ihr Aufbau ist grundsätzlich identisch mit dem der Kinozilien – inklusive der 9 × 2 + 2-Struktur. Der entscheidende Unterschied liegt vor allem in der Länge: Geißeln sind deutlich länger. Beim Menschen findet man sie praktisch nur am Spermium.
Mikrovilli
Mikrovilli sind fingerförmige Ausstülpungen der Zellmembran, die die Oberfläche einer Zelle deutlich vergrößern. Liegen viele Mikrovilli dicht beieinander, spricht man von einem Bürstensaum.
Sie sind ungefähr 0,08 µm dick und etwa 1–4 µm lang. Im Zentrum enthält jede Mikrovillus ein Bündel aus Aktinfilamenten. Diese Aktinfilamente sind in einem dichten Aktinnetzwerk verankert, das den Mikrovilli Stabilität und Halt gibt.
Funktionell sind Mikrovilli besonders wichtig für die Resorption. Man findet sie daher typischerweise dort, wo Stoffaufnahme eine zentrale Rolle spielt, z. B. im Dünndarm oder auch im Plexus choroideus.

Zellkontakte #
Zellen in Geweben liegen nicht einfach „nebeneinander“, sondern sind über spezialisierte Strukturen miteinander verbunden. Diese Zellkontakte erfüllen drei Grundaufgaben: Sie dichten Zellverbände ab, sie verleihen Geweben mechanische Stabilität und sie ermöglichen direkte Kommunikation zwischen Nachbarzellen. Besonders wichtig sind Zellkontakte in Epithelien, weil dort eine stabile Barriere mit klarer Polarität (apikal vs. basal) entstehen muss.
Man unterscheidet funktionell drei große Gruppen: Verschlusskontakte, Haftkontakte und Kommunikationskontakte.
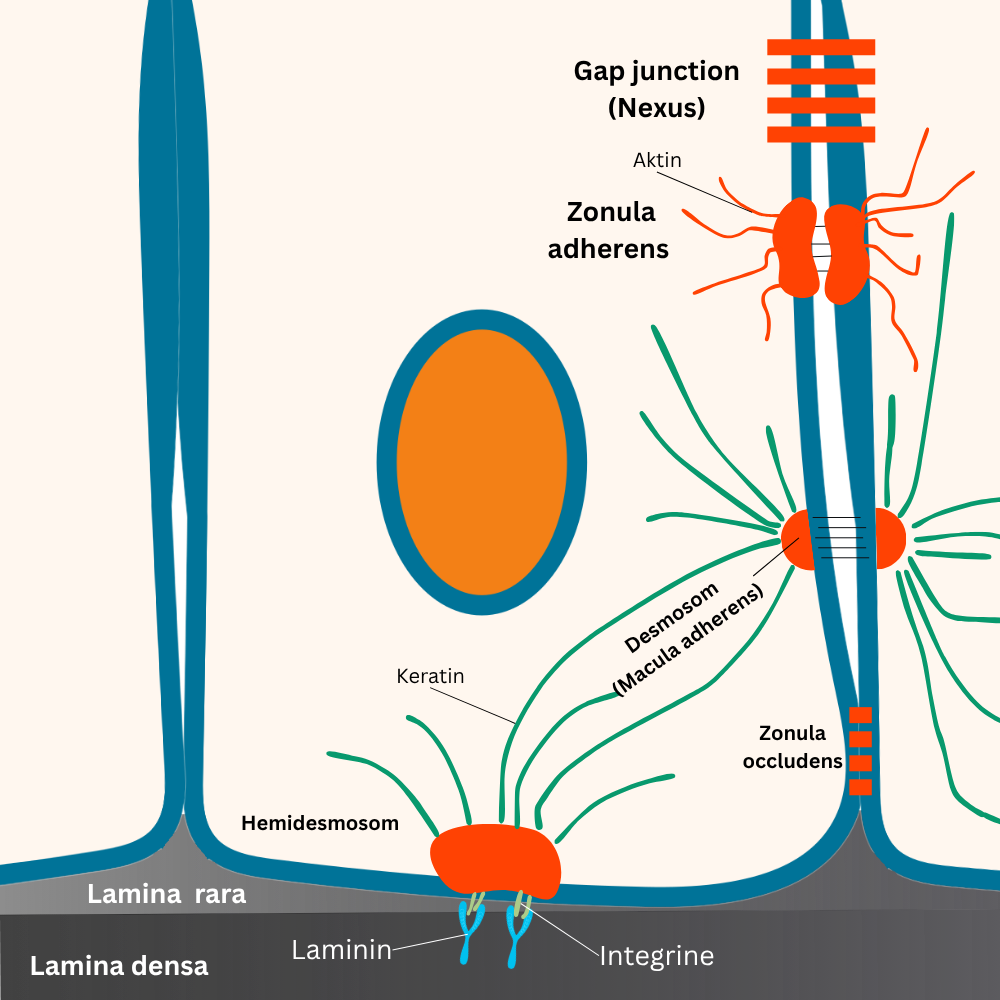
Verschlusskontakte
Verschlusskontakte (Tight Junctions) liegen typischerweise sehr apikal in Epithelzellen und bilden eine Art „Dichtungsring“ um die Zelle. Ihre zentrale Aufgabe ist es, den parazellulären Weg (also den Weg zwischen zwei Zellen) zu kontrollieren. Dadurch wird festgelegt, welche Stoffe überhaupt zwischen den Zellen hindurchtreten dürfen. Je nach Gewebe können Tight Junctions sehr dicht sein (starke Barriere) oder etwas „durchlässiger“ (gezielte, kontrollierte Passage).
Neben der Abdichtung haben sie eine zweite wichtige Funktion: Sie sichern die Zellpolarität, indem sie verhindern, dass Membranproteine unkontrolliert zwischen apikaler und basolateraler Membrandomäne „durchmischen“. Damit bleibt die funktionelle Aufteilung der Zelloberfläche erhalten.
Haftkontakte
Haftkontakte sorgen dafür, dass Zellen Kräfte aufnehmen, weitergeben und als Verband stabil bleiben. Je nachdem, ob Zellen aneinander oder an die extrazelluläre Matrix gebunden werden, unterscheidet man unterschiedliche Kontaktformen. Gemeinsam ist ihnen, dass sie innen an das Zytoskelett gekoppelt sind und so mechanische Belastungen abfangen können.
Eine wichtige Gruppe sind Kontakte, die vor allem mit Aktinfilamenten verbunden sind. Sie stabilisieren Zellschichten und helfen, Zugkräfte entlang eines Gewebes zu verteilen. Daneben gibt es Kontakte, die vor allem mit Intermediärfilamenten gekoppelt sind. Diese sind besonders robust und machen Gewebe widerstandsfähig gegenüber mechanischem Stress.
Sehr typisch sind Desmosomen: Das sind punktförmige „Nieten“ zwischen zwei Nachbarzellen. Sie verankern Intermediärfilamente und sind besonders in Geweben wichtig, die hohe mechanische Belastung aushalten müssen, zum Beispiel in der Haut oder im Herzgewebe.
Davon abzugrenzen sind Hemidesmosomen. Sie verbinden nicht zwei Zellen miteinander, sondern verankern eine Zelle an der Basalmembran bzw. an der extrazellulären Matrix. Funktionell ist das die feste „Befestigung“ der Zelle am Untergrund, was vor allem für Epithelien entscheidend ist.
Kommunikationskontakte
Kommunikationskontakte (Gap Junctions) ermöglichen den direkten Austausch zwischen Nachbarzellen. Dabei bilden Membranproteine beider Zellen zusammen einen Kanal, der die Zytoplasmen miteinander verbindet. So können kleine Moleküle und Ionen direkt von einer Zelle zur nächsten gelangen. Das ist besonders wichtig, wenn Zellen ihre Aktivität synchronisieren müssen.
Ein klassisches Beispiel ist das Herz: Hier trägt die direkte elektrische Kopplung über solche Kontakte dazu bei, dass sich Erregungen schnell ausbreiten und die Kontraktion koordiniert abläuft. Auch in anderen Geweben sind Gap Junctions wichtig, um Stoffwechsel- und Signalzustände zwischen Zellen abzustimmen.
Zelltod #
Zellen sind nicht darauf ausgelegt, „für immer“ zu überleben. In einem Organismus müssen Zellen gezielt entfernt werden können – entweder, weil sie nicht mehr gebraucht werden, weil sie beschädigt sind oder weil sie eine Gefahr darstellen. Grundsätzlich unterscheidet man zwei wichtige Formen des Zelltods: Apoptose und Nekrose. Beide führen zum Absterben der Zelle, unterscheiden sich aber deutlich in Ablauf, Morphologie und Konsequenzen für das umliegende Gewebe.
Apoptose
Die Apoptose ist ein programmierter, kontrollierter Zelltod. Sie ist ein normaler Bestandteil der Entwicklung und Gewebeerneuerung und dient auch der Qualitätskontrolle: Zellen mit irreparablen DNA-Schäden, falsch gefalteten Proteinen oder gefährlicher Entgleisung können so „sauber“ entfernt werden.
Typisch ist, dass die Zelle dabei schrumpft, ihr Zellkern Chromatin kondensiert und die DNA in geordneten Schritten zerlegt wird. Die Zellmembran bleibt zunächst intakt, bildet aber Ausstülpungen (Blebs). Am Ende zerfällt die Zelle in kleine, membranumhüllte Apoptosekörperchen, die von Nachbarzellen oder Fresszellen rasch aufgenommen werden. Weil der Zellinhalt nicht unkontrolliert austritt, entsteht dabei kaum bis keine Entzündungsreaktion.
Molekular wird die Apoptose vor allem durch Caspasen gesteuert (Proteasen, die gezielt Zellbestandteile spalten). Ausgelöst werden kann sie über zwei zentrale Wege: Ein intrinsischer (mitochondrialer) Weg, der bei innerem Stress wie DNA-Schaden oder Sauerstoffmangel aktiviert wird, und ein extrinsischer Weg über Todesrezeptoren an der Zelloberfläche. Beide Wege münden in eine Caspase-Kaskade, die die Zelle kontrolliert abbaut.

Nekrose
Die Nekrose ist im klassischen Verständnis ein unkontrollierter, meist durch starke äußere Einwirkung ausgelöster Zelltod, zum Beispiel durch schwere mechanische Schäden, Toxine, extreme Hitze/Kälte oder ausgeprägte Durchblutungsstörungen. Hier verliert die Zelle ihre Homöostase: Wasser strömt ein, die Zelle schwillt an, Organellen werden funktionsunfähig und schließlich reißt die Zellmembran.
Dadurch tritt Zellinhalt in das umliegende Gewebe aus. Genau das ist der entscheidende Punkt: Diese freigesetzten Bestandteile wirken als Gefahrensignale und führen typischerweise zu einer Entzündungsreaktion. Nekrose betrifft deshalb nicht nur die einzelne Zelle, sondern kann das umliegende Gewebe stark mitbetreffen und zusätzliche Schäden nach sich ziehen.
Apoptose vs. Nekrose
Wenn du dir nur ein Unterscheidungsprinzip merken willst: Apoptose ist ein „aufgeräumter“, energieabhängiger Selbstabbau mit intakter Membran bis spät und ohne Entzündung; Nekrose ist ein „chaotischer“ Zerfall mit frühem Membranverlust, Austritt von Zellinhalt und Entzündung im Gewebe.
